
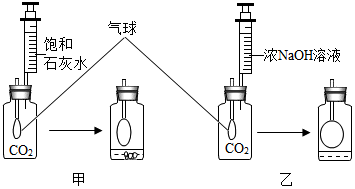
 【发现问题】研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液.
【发现问题】研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液.分析 【现象结论】根据甲装置中产生的实验现象出现白色沉淀,说明通常用饱和石灰水检验CO2;由反应现象知:甲、乙两装置的气球,乙的气球变化大,说明瓶内压强小,二氧化碳被吸收的多;
【计算验证】根据控制变量法的具体操作进行分析;
【思考评价】小李同学的结论不正确,考虑Ca(OH)2微溶于水,而NaOH易溶于水,Ca(OH)2的饱和溶液远没有等质量的NaOH的饱和溶液含溶质的质量多.
解答 解:【现象结论】根据甲、乙装置中产生的实验现象甲装置中石灰水变浑浊,乙装置中无现象,二氧化碳与澄清的石灰水反应生成碳酸钙沉淀,通过这一现象,可以用澄清的石灰水来检验二氧化碳的存在,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;比较甲、乙两装置的实验现象可以看出,乙中气球变化大,说明瓶内压强小,二氧化碳被吸收的多,则吸收CO2的量甲<乙;
【计算验证】依据控制变量法的具体操作可知,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH;
【思考评价】另一位同学小李同学通过计算结果发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH.因此,他认为通常吸收CO2应该用饱和石灰水,小张的结论不正确.尽管理论上Ca(OH)2比等质量的NaOH吸收的CO2多,但由于Ca(OH)2微溶于水,而NaOH易溶于水,Ca(OH)2的饱和溶液远没有等质量的NaOH的饱和溶液含溶质的质量多,因此也没有NaOH的饱和溶液吸收CO2 的质量多,所以应用NaOH溶液吸收.
故答案为:【现象结论】CO2+Ca(OH)2=CaCO3↓+H2O;CO2与石灰水作用有明显实验现象,NaOH无明显现象;气球体积增大,溶液不变浑浊;乙;
【计算验证】等质量;
【思考评价】不正确,因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中溶质的质量分数很小.
点评 本题考查了二氧化碳的检验,掌握酸碱盐的溶解性是解答的关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
 2013年12月2日1时30分,搭载着“嫦娥”三号的“长征”三号乙运载火箭在西昌卫星发射中心成功发射升空并准确入轨.航天所用燃料之一为氢气.纯净的氢气在空气中燃烧,下列现象不符合事实的是( )
2013年12月2日1时30分,搭载着“嫦娥”三号的“长征”三号乙运载火箭在西昌卫星发射中心成功发射升空并准确入轨.航天所用燃料之一为氢气.纯净的氢气在空气中燃烧,下列现象不符合事实的是( )| A. | 产生黄色火焰 | |
| B. | 用冷而干燥的烧杯罩在火焰上方,烧杯内部有水珠生成 | |
| C. | 接触罩在火焰上的烧杯感到发烫 | |
| D. | 将罩在火焰上方的烧杯倒置并迅速加入少量石灰水后,石灰水一定变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
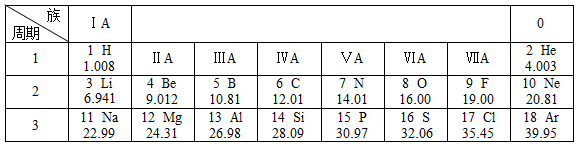
| A. | 最外层电子数为8的粒子,一定是稀有气体元素的原子 | |
| B. | 从元素周期表中可以查出元素的相对原子质量 | |
| C. | 过氧化氢溶液与二氧化锰混合,二氧化锰能加快过氧化氢分解速率 | |
| D. | 地壳中含量最多的金属元素是Al、最多的非金属元素是O |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
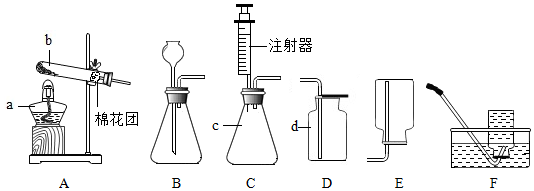
科目:初中化学 来源: 题型:实验探究题
 用如图所示装置测定空气中氧气的含量.请回答有关问题:
用如图所示装置测定空气中氧气的含量.请回答有关问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com