
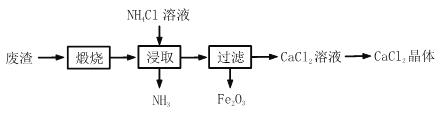
【题目】某工厂产生的废渣主要成分是 CaCO3(杂质为 Fe2O3)。用该废渣制取 CaCl2 晶 体(CaCl2xH2O)并进行组成测定,其制取的流程如下图所示:
资料:NH4Cl 溶液显酸性,且浓度越高酸性越强
(1)写出煅烧时发生反应的化学方程式_____。
(2)浸取时主要发生了两个反应,分别是:CaO + H2O = Ca(OH)2 和_____。生成的NH3 能使湿润的红色石蕊试纸变_____色。
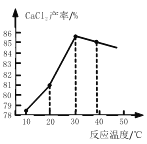
(3)在其它条件相同的情况下,CaCl2 的产率随浸取温度的变化如图所示,则宜选择的浸取温度为_____左右。
(4)若使用过量浓度较高的 NH4Cl 溶液,则所得 CaCl2 溶液中会含有 NH4Cl、_____(填化学式)等杂质。
(5)为测定晶体(CaCl2xH2O)的组成,进行如下实验:
a.称取 14.7g CaCl2xH2O 晶体于锥形瓶内,加入适量蒸馏水。使其全部溶解。
b.再向其中加入足量的 Na2CO3 溶液,静置。
c.过滤、洗涤、干燥、称量,得到 10.0g 固体。
①判断该步骤 b 中沉淀是否完全的方法是:静置,取少量上层清液,滴加_____溶液,若没有沉淀产生,则说明已沉淀完全。
② CaCl2xH2O 中,x=_____。
【答案】CaCO3![]() CaO+CO2↑ Ca(OH)2 +2NH4Cl=CaCl2+2NH3↑+2H2O 蓝 30℃ FeCl3 碳酸钠 2
CaO+CO2↑ Ca(OH)2 +2NH4Cl=CaCl2+2NH3↑+2H2O 蓝 30℃ FeCl3 碳酸钠 2
【解析】
(1)煅烧时发生反应的化学方程式CaCO3高温CaO+CO2↑。
(2)浸取时主要发生了两个反应,分别是:CaO + H2O = Ca(OH)2 和Ca(OH)2 +2NH4Cl=CaCl2+2NH3↑+2H2O。生成的NH3 能使湿润的红色石蕊试纸变蓝色。
(3)30℃时,CaCl2 的产率最高,则宜选择的浸取温度为30℃左右。
(4)NH4Cl溶液显酸性,且浓度越高酸性越强酸与氧化铁反应生成氯化铁,杂质是氯化铁:FeCl3;
(5)①沉淀完全说明溶液中不含有氯化钙,如果向上层清液中滴加碳酸钠,没有沉淀产生,说明已沉淀完全;
②设晶体样品中CaCl2的质量为a,则
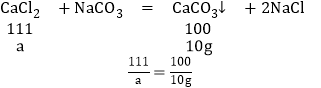
所以水的质量=14.7g-11.1g=3.6g
由CaCl2xH2O晶体中CaCl2和水的质量比可列式:![]()
x=2。


 阶梯计算系列答案
阶梯计算系列答案科目:初中化学 来源: 题型:
【题目】推理是学习化学的一种重要方法。下列推理合理的是( )
A. 离子是带电的粒子,带电的粒子一定是离子
B. 单质是由同种元素组成的,则只含一种元素的纯净物,一定是单质
C. 置换反应有单质和化合物生成,则有单质和化合物生成的反应,一定是置换反应
D. 溶液具有均一性和稳定性,则有均一性和稳定性的液体一定是溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请回答下列有关金属的问题。
(1)铝是活泼金属,为什么通常铝锅却很耐腐蚀_____?
(2)如图是某探究实验装置图。一段时间后,能观察到什么现象_____?(装置气密性良好,且开始时U型管两端的红墨水液面相平)
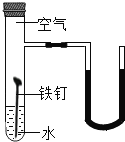
(3)X、Y、Z是三种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化。
①判断X、Y、Z和银四种金属的活动性由强到弱的顺序_____。
②具体确定一种X后,写出X与硝酸银溶液反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)某研究性学习小组为验证“氨气还原氧化铜”的实验,认真阅资料并做出以下准备。
资料准备:I.氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,溶液呈碱性。
Ⅱ.氨气还原氧化铜的化学反应原理:2NH3+3CuO![]() 3Cu+N2+3H2O。
3Cu+N2+3H2O。
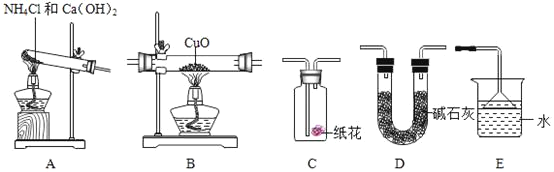
实验准备:
请回答:
①为达成“氨气还原氧化铜”的实验目的,装置A、B、D、E的正确连接顺序_____;(填序号)
②装置A中发生反应的化学方程式_____;
③装置B观察到的现象_____,装置E的作用_____;
④将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变蓝色,原因是_____。
(2)金属镁可与热水反应生成氢氧化镁和氢气,所得溶液呈碱性,可使酚酞溶液显紅色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气中一段时间后,发现溶液的红色褪去了。
①镁与热水反应的化学方程式是_____。
②查阅资料:溶液红色褪去的原因是溶液碱性减弱。
(提出问题)导致溶液碱性减弱的原因是什么?
(假设与分析)
假设1:可能是氢氧化镁与N2或O2发生了反应。
假设2:可能是溶液吸收了空气中的_____。
假设3:可能是氢氧化镁的溶解度随温度的降低而_____。
由碱的性质可知,假设1不成立。
(实验探究)
实验操作 | 实验现象 | 结论 |
(1)取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象。 | _____ | 假设2成立 |
(2)取上述红色溶液,_____,_____,观察现象。 | 红色褪去 | 假设3成立 |
(拓展延伸)
③将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。
请解释其原因:_____。
④除上述金属外,根据金属活动性顺序,预测_____也能跟硫酸铜溶液反应产生上述现象(举一例即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学学习中,我们发现所学的化学知识可以帮助解决很多生活中的问题。
(1)如果发现自家种的植物叶色发黄,可以给植物施加含有_____元素的化肥。
(2)用洗洁精洗刷碗筷上的油污,是利用洗洁精的_____作用。
(3)生活中可通过煮沸来降低水的硬度,其中一个化学反应是,Ca(HCO3)2 在加热的条件 下分解生成一种难溶性的物质、水和二氧化碳,从而降低水中 Ca2+的浓度。其中的化学方程式是_____。
(4)使用燃气灶具时,发现灶具火焰呈黄色,锅底出现黑色物质,原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向100g质量分数为3.65%的盐酸中逐滴加入4%的氢氧化钠溶液,同时测定有关数据下列图象正确的是(横坐标为每次加入氢氧化钠溶液的量)( )
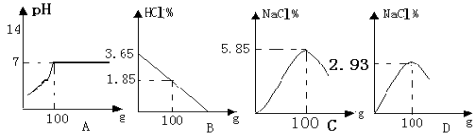
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示。下列说法错误的是( )

A. t2℃时,甲物质的溶解度大于乙物质的溶解度
B. t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g
C. t1℃时,甲、乙两种物质的溶液的溶质质量分数一定相等
D. t2℃时等质量的甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
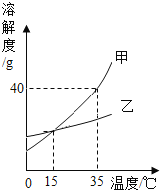
A. 15℃时,甲和乙的饱和溶液中溶质质量相等
B. 35℃时,30g甲加入50g水中,得到80g甲溶液
C. 从乙溶液中获得乙晶体,常用蒸发结晶的方法
D. 降低温度,甲溶液中溶质的质量分数一定减小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象与对应操作过程不相符的是( )
A. 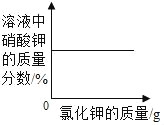 向饱和硝酸钾溶液中加入氯化钾
向饱和硝酸钾溶液中加入氯化钾
B. 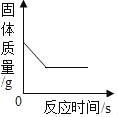 高温条件下CO与Fe2O3反应
高温条件下CO与Fe2O3反应
C. 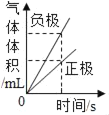 电解水实验中两极气体的体积关系
电解水实验中两极气体的体积关系
D. 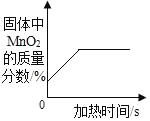 加热氯酸钾与二氧化锰的混合物
加热氯酸钾与二氧化锰的混合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com