
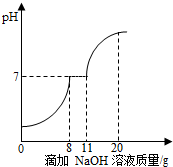
 在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是因为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),同学们做了如下实验:取10g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.
在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是因为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),同学们做了如下实验:取10g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.分析 在盐酸存在的条件下,不能形成氢氧化铁沉淀,所以只有把盐酸消耗掉之后,才会生成沉淀,从图中可知与氯化铁反应的氢氧化钠的质量,然后根据氯化铁和氢氧化钠反应的化学方程式可以计算出氯化铁的质量,进而求算出该工业盐酸中氯化铁的溶质质量分数.
解答 解:(1)在盐酸存在的条件下,不能形成氢氧化铁沉淀,只有把盐酸消耗掉之后,才会生成沉淀,根据图中信息可知:在氢氧化钠溶液被消耗至8g时,开始产生沉淀,说明此时盐酸被消耗完全,而消耗氢氧化钠溶液11g时不再产生沉淀,所以可以判断与氯化铁反应的氢氧化钠溶液的质量为11g-8g=3g,故填:3;
(2)与氯化铁反应消耗氢氧化钠的质量为:3g×10%=0.3g
设10g该工业盐酸中氯化铁的质量为x
FeCl3+3NaOH═Fe(OH)3↓+3NaCl
162.5 120
x 0.3g
$\frac{162.5}{120}=\frac{x}{0.3g}$
解得:x=0.40625g
该工业盐酸中氯化铁的质量分数为
$\frac{0.40625g}{10g}$×100%=4.1%
答:该工业盐酸中氯化铁的质量分数为4.1%.
点评 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识按照题目要求进行认真地选择或解答即可.


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:初中化学 来源: 题型:填空题
| 实 验 方 法 | 实 验 现 象 和 结 论 |
| 分别取一定量的两种样品加适量熟石灰研磨 | 闻到刺激性氨味的是NH4Cl,无味的是K2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | KCl | NH4Cl | CaCl2 | ① |
| 现象 | 继续发生反应生成二氧化碳气体,但反应较慢,反应一段时间后就趋于停止. | CaCl2溶解并生成大量的白色固体,但不能继续发生反应 | 没有明显 可见的现象 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 物 质 | 选用试剂 | 操作 |
| A | CO2(CO) | O2 | 点燃 |
| B | NaOH溶液(Na2CO3) | 稀盐酸 | 加入试剂至不再产生气泡 |
| C | KNO3溶液(KOH) | Cu(NO3)2溶液 | 加入适量的试剂,直接蒸发 |
| D | CaCl2溶液(HCl) | 过量CaCO3 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盛放石灰水后留下的白色固体 | |
| B. | 氯化铜溶液与氢氧化钠溶液反应后留下的蓝色固体 | |
| C. | 碱式碳酸铜受热分解后的黑色固体 | |
| D. | 用一氧化碳还原氧化铜后留下的红色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 序号 | 实验步骤 | 实验现象 |
| ① | 观察溶液 | 无色液体 |
| ② | 取少量该溶液于试管中,滴加紫色石蕊试液 | 紫色石蕊试液变蓝色 |
| ③ | 另取少量溶液在酒精灯火焰上灼烧 | 火焰呈现黄色 |
| ④ | 取少量该溶液于试管中,先滴加硫酸铜溶液,再滴加稀盐酸 | 先有蓝色沉淀生成,加入稀盐酸后沉淀消失,无其它明显现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
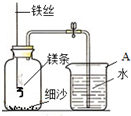 探究一:某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
探究一:某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.| 实验序号 | H2O2溶液浓度% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 0 | 2 | 10.76 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com