
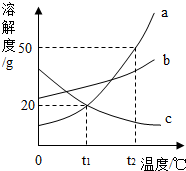
 a、b、c三种固体物质的溶解度曲线如图所示,下列叙述中正确的是B.
a、b、c三种固体物质的溶解度曲线如图所示,下列叙述中正确的是B.分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液的质量;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液是否饱和.
解答 解:A.由溶解度曲线可知,一定温度下,a物质的溶解度大于b物质的溶解度,一定温度下,a物质的溶解度小于b物质的溶解度,该选项说法不正确;
B.因为由t2℃冷却到t1℃时,a物质的溶解度差大于b物质的溶解度差,并且t1℃时b的溶解度大于a的溶解度,因此将t2℃质量分数相同的a、b的溶液分冷却到t1℃,所得溶液的质量分数a不可能大于b,该选项说法正确;
C.t2℃时,a的溶解度是50g,30ga物质加入50g水中,能够溶解25g,得到75g溶液,该选项说法不正确;
D.t2℃时,a的溶解度大于b的溶解度,b的溶解度大于c的溶解度,将等质量的a、b、c分别加入100g水中,充分溶解后只有一种未达饱和,该物质应该是溶解度最大的物质,即a物质.
故选:B;
故填:a.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案科目:初中化学 来源: 题型:填空题
 图中,A代表地壳中含量第二位的金属,C为黑色粉末,E在常温下为液态且为相对分子质量最小的氧化物.常温下,相连环物质间能发生反应,请填空.
图中,A代表地壳中含量第二位的金属,C为黑色粉末,E在常温下为液态且为相对分子质量最小的氧化物.常温下,相连环物质间能发生反应,请填空.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 序号 | 过氧化氢 的质量分数 | 过氧化氢 溶液体积(mL) | 温度 | 二氧化锰 的用量/g | 收集氧气 的体积/ml | 反应所需 的时间/s |
| ① | 5% | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15% | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30% | 5 | 35 | 2 | 49.21 | |
| ④ | 30% | 5 | 55 | 2 | 10.76 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事实 | 解释 |
| A | 酒精灯不用时,需用灯帽盖好 | 酒精分子不断运动到空气中 |
| B | 金刚石比石墨硬度大 | 碳原子的结构不同 |
| C | 氯化氢溶液导电 | 氯化氢由分子构成,且能自由移动 |
| D | 酒精溶液是混合物 | 所含原子种类不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳.
某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳.| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用工业盐亚硝酸钠烹调食物 | |
| B. | 用煮沸的方法降低水的硬度 | |
| C. | 室内起火时,立即打开所有门窗进行呼救 | |
| D. | 冬天在室内用炭烤火取暖时,关闭门窗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com