
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.90 | 97.80 | 116.70 | 135.60 | 155.05 | 175.05 | 195.05 |
分析 根据表格中所给数据可知,当加盐酸到第五次之后,物质的质量不在发生变化,说明此时样品全部反应,生成的二氧化碳质量也恒定不变,由此根据化学方程式进行计算即可.
解答 解:(1)每次加入20g稀盐酸,那么按理来说第2次烧杯及所称物质总质量应为78.9g+20g=98.90g,可只有97.80g,所以生成了二氧化碳98.90g-97.80g=1.1g,这是第一次,前4次每加一次生成二氧化碳1.1g,最后一次因碳酸钠反应完,所以生成二氧化碳135.6g+20g-155.05g=0.55g,5次一共生成了1.1g×4+0.55g=4.95g.
仔细观察数据,会发现第6次与第5次数据差还是20g,这说明稀盐酸没有被反应,所以第5次加稀盐酸时,碳酸钠已反应完.但注意,第5次20g稀盐酸没有反应完;故填:5;4.95;
(2)设12g样品中碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.95g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{4.95g}$
x=11.925g
y=13.16g
样品中碳酸钠的质量分数=$\frac{11.925g}{12g}$×100%=99.4%;
(3)经过分析题意可知,每加入20g稀盐酸完全反应时,生成1.1g CO2,第五次加入20g稀盐酸生成0.55g CO2,说明有10g稀盐酸参加了反应,所以参加反应的盐酸总质量为90g.
样品与稀盐酸恰好完全反应时所得溶液中溶质的质量分数=$\frac{12g-11.925g+13.16g}{12g+90g-4.95g}$×100%=13.6%
答:(2)样品中碳酸钠的质量分数为99.4%;(3)样品与稀盐酸恰好完全反应时所得溶液中溶质的质量分数为13.6%.
点评 本题是一道化学方程式和图表相结合在一起的计算题,难度较大,对学生的审题和理解能力较高.


科目:初中化学 来源: 题型:解答题
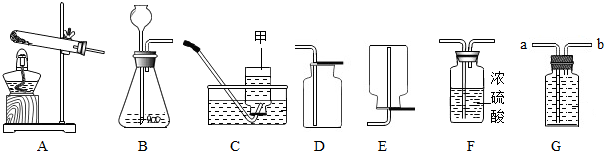
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
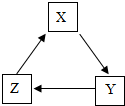 下列各组物质通过一步反应就能实现如图转化的是( )
下列各组物质通过一步反应就能实现如图转化的是( )| X | Y | Z | |
| A | H2O | O2 | CO2 |
| B | Ca(OH)2 | NaOH | NaCl |
| C | AgNO3 | Ba(NO3)2 | BaSO4 |
| D | Fe | FeCl2 | Fe2O3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生成气体的质量可能是11克或33克 | |
| B. | 滤渣中的红色物质可能是32克或96克 | |
| C. | 参与反应的氧化铜质量可能是40克或120克 | |
| D. | 稀硫酸的溶质质量可能是38.4克或115.2克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有机合成材料都是高分子材料 | |
| B. | 焚烧聚乙烯塑料会造成环境污染 | |
| C. | 使用过的塑料、橡胶应回收利用 | |
| D. | 棉花、羊毛、聚乙烯、橡胶都是合成材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com