
| 步 骤 | 现 象 | 结 论 |
| 取反应后的红色固体装入试管, 滴入足量的稀硫酸,充分反应 | 红色固体部分减少, 溶液变为蓝色 色 | 红色固体的成分既有Cu也有Cu2O |
分析 【查阅资料】(1)根据反应物、生成物的特点分析反应类型;
【实验过程】根据物质的性质及相互间的反应、实验现象进行分析解答;
【思考】根据微型实验装置药品用量较少,节约药品分析.
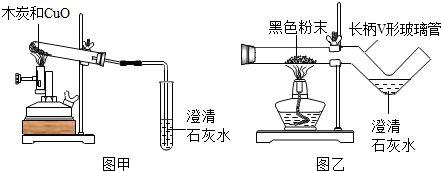
解答 解:【查阅资料】(1)根据化学方程式C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑可知,木炭和氧化铜的反应是氧化还原反应;
【实验过程】木炭和氧化铜的反应生成铜单质,铜不与稀硫酸反应,由资料可知,Cu2O是红色固体,且能与稀硫酸反应.因此,待玻璃管冷却后,提取里面的红色固体装入试管中,然后向里面滴入足量的稀硫酸,进行观察,这时会看到红色固体部分减少,且溶液变为蓝色,这说明红色固体的成分既有Cu也有Cu2O.
【思考】图乙装置与使用图甲装置相比,图乙装置是微型实验装置,药品用量较少,可节约药品;
故答案为:【查阅资料】氧化还原反应;
【实验过程】稀硫酸;蓝色;红色固体的成分既有Cu也有Cu2O.
【思考】节约药品;
点评 有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便.


科目:初中化学 来源: 题型:解答题
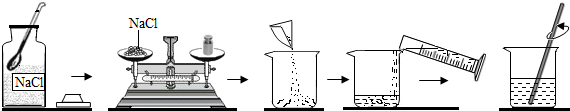
 3月22日是“世界水日”.水与人类的生活和生产密切相关.请回答以下问题:
3月22日是“世界水日”.水与人类的生活和生产密切相关.请回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间(分钟) | 0.5 | 1 | 1.5 | 2 | 2.5 | 3 | 3.5 | 4 |
| 二氧化碳(mL) | 40 | 70 | 95 | 110 | 116 | 120 | 120 | 120 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com