
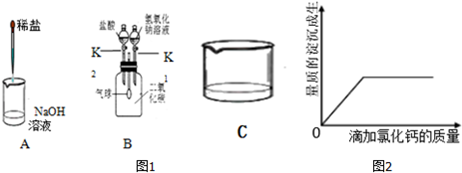
分析 (1)从化学方程式书写角度思考;
(2)氢氧化钠与盐酸反应生成氯化钠和水,打开K1时,氢氧化钠和二氧化碳反应,使瓶内压强减小,在大气压的作用下,气球鼓起,打开K2时,盐酸与反应生成的碳酸钠反应生成二氧化碳,使瓶内的压强增大,小气球变瘪,根据方程式的书写方法写出方程式;
(3)根据两个反应可以判断含有的物质有哪些,溶液呈红色,则碱性物质为氢氧化钠或碳酸钠,根据与氯化钙反应的图象分析得出合理的结论.
解答 解:(1)实验A:此反应的反应物是氯化氢和氢氧化钠,生成物是氯化钠和水;故答案为:HCl+NaOH═NaCl+H2O;
(2)B实验中,打开K1时,氢氧化钠和二氧化碳反应,生成碳酸钠和水,使瓶内压强减小,在大气压的作用下,气球鼓起,打开K2时,盐酸与反应生成的碳酸钠反应生成二氧化碳,使瓶内的压强增大,小气球重新变瘪;氢氧化钠与二氧化碳反应的反应物是氢氧化钠和二氧化碳,写在等号的左边,生成物是碳酸钠和水,写在等号的右边,用观察法配平即可,所以方程式是:2NaOH+CO2=Na2CO3+H2O;
故答案为:打开K1,气球逐渐鼓起(变大),(关闭K1),打开K2,有大量气泡产生,且气球逐渐变瘪(变小);2NaOH+CO2=Na2CO3+H2O;
(3)两个反应中均有氯化钠生成,所以一定含有氯化钠,氢氧化钠和碳酸钠均呈碱性,可能同时存在,CaCl2+Na2CO3=CaCO3↓+2NaCl,从图象可以看出,加入氯化钙溶液就有沉淀生成,废液中一定含有碳酸钠,不可能只是氢氧化钠,要判断是否含有氢氧化钠,可以根据碳酸钠完全反应后的溶液是否仍为红色来确定.
故答案为:NaCl;碳酸钠和氢氧化钠;A;据图可知,加入氯化钙溶液就有沉淀生成,废液中一定含有碳酸钠.若加入过量氯化钙溶液废液红色褪去则不含氢氧化钠,若仍呈红色则含氢氧化钠
点评 本题考查了氢氧化钠和盐酸的反应,以及氢氧化钠和二氧化碳的反应,完成此题,可以依据氢氧化钠的化学性质进行.所以要求同学们在平时的学习中加强基础知识的储备.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | 合金 | 不锈钢、焊锡、生铁 |
| B | 干燥剂 | 浓硫酸、生石灰、氢氧化钠固体 |
| C | 碱类 | 烧碱、纯碱、熟石灰 |
| D | 合成材料 | 合成橡胶、合成纤维、塑料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | Fe+CuSO4═Cu+FeSO4 | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | CO2+Ca(OH)2═CaCO3↓+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
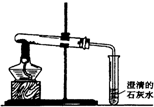 由C、CuO、Fe三种物质组成的混合物,放在试管中,如图所示高温加热.当观祭到澄清石灰水变浑浊时,停止加热,密封冷却至室温;然后往试管中加入稀硫酸,观察到有气泡冒出,且红色物质明显增加.请根据这些信息,推断红色物质产生和增加的可能的原因(用化学万程式表) 产生红色物质的原因C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
由C、CuO、Fe三种物质组成的混合物,放在试管中,如图所示高温加热.当观祭到澄清石灰水变浑浊时,停止加热,密封冷却至室温;然后往试管中加入稀硫酸,观察到有气泡冒出,且红色物质明显增加.请根据这些信息,推断红色物质产生和增加的可能的原因(用化学万程式表) 产生红色物质的原因C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③④⑤ | C. | ③④⑤⑥ | D. | ①③④⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
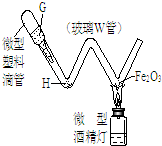 如图为某种“微型”实验装置.如果G处装稀盐酸,H处放少量铁屑,则加热处的现象为红色粉末变黑色,(已知H2和CO相似可以将铁从Fe2O3中还原出来),发生反应的化学方程式为:Fe2O3+3H2$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O.用微型仪器进行实验,除试剂用量极少以外,还可能具有的优点是产生废物少,减少对环境的污染(其他合理答案也可) (写一点)..
如图为某种“微型”实验装置.如果G处装稀盐酸,H处放少量铁屑,则加热处的现象为红色粉末变黑色,(已知H2和CO相似可以将铁从Fe2O3中还原出来),发生反应的化学方程式为:Fe2O3+3H2$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O.用微型仪器进行实验,除试剂用量极少以外,还可能具有的优点是产生废物少,减少对环境的污染(其他合理答案也可) (写一点)..查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com