
 一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力.下面就让我们一起回顾硫酸型酸雨形成的模拟实验:
一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力.下面就让我们一起回顾硫酸型酸雨形成的模拟实验:| 测定时间 | 8:00 | 8:10 | 8:20 | 8:30 |
| pH | 4.94 | 4.88 | 4.86 | 4.85 |
| ||
| ||


科目:初中化学 来源: 题型:
 (1)饮用酸碱度过大或硬度过大的水都不利于人体健康,可用
(1)饮用酸碱度过大或硬度过大的水都不利于人体健康,可用查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 某同学称取一定质量的铁粉样品(含有少量不与稀硫酸反应,也不溶于水的固体杂质)于烧杯中,加入9.8%的稀硫酸100g,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题:
某同学称取一定质量的铁粉样品(含有少量不与稀硫酸反应,也不溶于水的固体杂质)于烧杯中,加入9.8%的稀硫酸100g,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 1.0 | 1.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| 实验操作 | 实验现象 | 目的/结论 |
| ①取白色固体适量配制成溶液.往所得溶液中滴加过量的 | 有白色沉淀生成 | 除去白色固体中的 |
| ②取滤液,往滤液中滴入几滴 | 白色固体中没有氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:
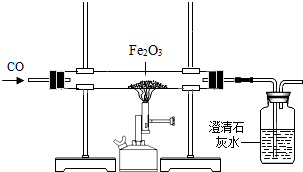 如图所示,用已经验纯的CO进行实验,
如图所示,用已经验纯的CO进行实验,查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com