
”¾ĢāÄæ”æij»Æѧ»ī¶ÆŠ”×éŗĻ×÷ѧĻ°ĒāŃõ»ÆÄĘŗĶĒāŃõ»ÆøʵÄĻą¹ŲÖŖŹ¶”£Čē±ķŹĒCa£ØOH£©2ŗĶNaOHµÄČܽā¶ČŹż¾Ż”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ĪĀ¶Č/”ę | 0 | 20 | 40 | 60 | 80 | 100 | |
Čܽā¶Č/g | Ca£ØOH£©2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
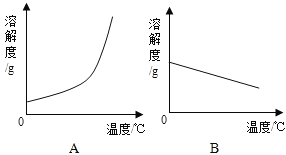
£Ø1£©ŅĄ¾ŻÉĻ±ķŹż¾Ż£¬»ęÖĘĮĖCa£ØOH£©2ŗĶNaOHµÄČܽā¶ČĒśĻߣ¬Ķ¼ÖŠÄܱķŹ¾NaOHČܽā¶ČĒśĻߵďĒ_____£ØĢī”°A”±»ņ”°B”±£©”£
£Ø2£©½«Ņ»Ęæ½Ó½ü±„ŗĶµÄCa£ØOH£©2ČÜŅŗ±ä³É±„ŗĶČÜŅŗ£¬¾ßĢå“ėŹ©ÓŠ£ŗ
¢Ł¼ÓČėŹŹĮæĒāŃõ»ÆøĘ¢ŚÉżøßĪĀ¶Č¢Ū½µµĶĪĀ¶Č¢Ü¼ÓČėĖ®¢ŻÕō·¢Ė®ŗóŌŁ»Öø“µ½ŌĪĀ¶Č¢Ž¼ÓČėŹŹĮæÉśŹÆ»Ņ”£
ĘäÖŠ“ėŹ©ŌŚŌĄķÉĻÕżČ·µÄŹĒ_____£ØĢī×ÖÄø£©
A ¢Ś¢Ü¢Ž B ¢Ū¢Ü C ¢Ł¢Ś¢Ż¢Ž D ¢Ł¢Ś¢Ż
£Ø3£©20”ꏱ£¬191g±„ŗĶNaOHČÜŅŗ£¬Õō·¢10gĖ®ŗó£¬ŌŁ»Öø“µ½20”ę£¬æÉĪö³öNaOH¹ĢĢ唣ÕāŹ±ČÜŅŗµÄÖŹĮæ·ÖŹżĪŖ_____
£Ø4£©20”ꏱ£¬Óū²ā¶ØNaOHČÜŅŗµÄpH£¬ČōĻČ½«pHŹŌÖ½ÓĆÕōĮóĖ®ČóŹŖ£¬ŌŁ½ųŠŠ²ā¶Ø£¬ŌņĖł²āČÜŅŗµÄpH_____£ØĢī”°Ę«“ó”±»ņ”°Ę«Š””±”°²»ŹÜÓ°Ļģ”±£©”£
£Ø5£©æɼų±šĒāŃõ»ÆÄĘČÜŅŗŗĶ³ĪĒåŹÆ»ŅĖ®µÄŅ»øö»Æѧ·“Ó¦·½³ĢŹ½ĪŖ_____”£
”¾“š°ø”æA C 47.6% Ę«Š” CO2+Ca£ØOH£©2£½CaCO3”ż+H2O
”¾½āĪö”æ
£Ø1£©ĒāŃõ»ÆøʵÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ų¼õŠ”£¬ĖłŅŌĶ¼ÖŠÄܱķŹ¾NaOHČܽā¶ČĒśĻߵďĒA£»
£Ø2£©ĒāŃõ»ÆøʵÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ų¼õŠ”£¬Ńõ»ÆøĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘ£¬ĖłŅŌ½«Ņ»Ęæ½Ó½ü±„ŗĶµÄCa£ØOH£©2ČÜŅŗ±ä³É±„ŗĶČÜŅŗ£¬¾ßĢå“ėŹ©ÓŠ£ŗ¢Ł¼ÓČėŹŹĮæĒāŃõ»ÆøĘ”¢¢ŚÉżøßĪĀ¶Č”¢¢ŻÕō·¢Ė®ŗóŌŁ»Öø“µ½ŌĪĀ¶Č”¢¢Ž¼ÓČėŹŹĮæÉśŹÆ»Ņ£¬ĘäÖŠ“ėŹ©ŌŚŌĄķÉĻÕżČ·µÄŹĒ¢Ł¢Ś¢Ż¢Ž£»
£Ø3£©20”ꏱ£¬191g±„ŗĶNaOHČÜŅŗ£¬Õō·¢10gĖ®ŗó£¬ŌŁ»Öø“µ½20”ę£¬æÉĪö³öNaOH¹ĢĢ壬ĒāŃõ»ÆÄĘČÜŅŗČŌŹĒ±ä»ÆČÜŅŗ£¬ĖłŅŌÕāŹ±ČÜŅŗµÄÖŹĮæ·ÖŹżĪŖ£ŗ![]() ”Į100%£½47.6%£»
”Į100%£½47.6%£»
£Ø4£©20”ꏱ£¬Óū²ā¶ØNaOHČÜŅŗµÄpH£¬ČōĻČ½«pHŹŌÖ½ÓĆÕōĮóĖ®ČóŹŖ£¬ČÜŅŗ¼īŠŌ¼õČõ£¬ŌŁ½ųŠŠ²ā¶Ø£¬ŌņĖł²āČÜŅŗµÄpHĘ«Š”£»
£Ø5£©¶žŃõ»ÆĢ¼ŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĢ¼ĖįÄĘŗĶĖ®£¬Ć»ÓŠĆ÷ĻŌĻÖĻ󣻶žŃõ»ÆĢ¼ŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĖ®£¬Éś³É°×É«³Įµķ£¬ĖłŅŌæɼų±šĒāŃõ»ÆÄĘČÜŅŗŗĶ³ĪĒåŹÆ»ŅĖ®µÄ·“Ó¦·½³ĢŹ½ĪŖ£ŗCO2+Ca£ØOH£©2£½CaCO3”ż+H2O”£


 ĄčĆ÷ĪÄ»Æŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
ĄčĆ÷ĪÄ»Æŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§Éč¼ĘČēĻĀĶ¼ĖłŹ¾ŹµŃ飬Ģ½¾æ¶žŃõ»ÆĢ¼µÄÓŠ¹ŲŠŌÖŹ”£
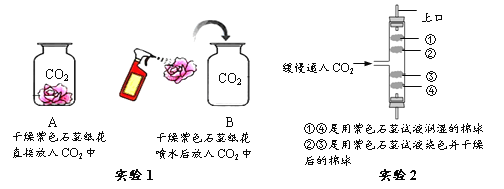
ŹµŃéŅ»£ŗAĘæÖŠ £ØŃ”Ģī”°ÄÜ”±»ņ”°·ń”±£©¹Ū²ģµ½ĻÖĻó£¬BĘæÖŠæɹŪ²ģµ½µÄĻÖĻóŹĒ ”£BĘæÖŠ³öĻÖĻÖĻóµÄŌŅņŹĒ£ØÓĆ»Æѧ±ķ“ļŹ½±ķŹ¾£© ”£øĆŹµŃé²ÉÓĆĮĖæĘѧĢ½¾æÖŠµÄæŲÖʱäĮæ·Ø£¬æŲÖʵıäĮæŹĒ ”£
ŹµŃ鶞£ŗ½«¶žŃõ»ÆĢ¼»ŗĀżĶØČėŹśÖ±·ÅÖĆµÄ²£Į§¹ÜÖŠ£¬ÄܹŪ²ģµ½µŚ £ØĢīŠņŗÅ£©ŗÅĆŽĒņĻȱäÉ«£¬ÓÉ“ĖĻÖĻóæÉÖŖ¶žŃõ»ÆĢ¼¾ßÓŠ µÄĪļĄķŠŌÖŹ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¼AŹĒÄĘŌŖĖŲŌŚŌŖĖŲÖÜĘŚÖÜĘŚ±ķÖŠµÄŠÅĻ¢£¬B”¢C”¢D·Ö±šŹĒČżÖÖŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼£¬øł¾ŻĢāÖŠŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©Ēė»³ö11ŗÅŌŖĖŲŌ×Ó½į¹¹Ź¾ŅāĶ¼_____£¬»Æѧ·“Ó¦ÖŠøĆŌ×Ó±Č½ĻČŻŅ×_____£ØĢī”°µĆµ½”±»ņ”°Ź§Č„”±£©µē×Ó±ä³ÉĄė×Ó£¬Ąė×Ó·ūŗÅĪŖ_____£®
£Ø2£©ČēĶ¼AĖłŹ¾£ŗÄĘŌ×ÓµÄŗĖµēŗÉŹżŹĒ_____£¬ÄĘŌ×ÓµÄĻą¶ŌŌ×ÓÖŹĮæŹĒ_____£®
£Ø3£©Ķ¼B”¢C”¢DÖŠ±ķŹ¾½šŹōŌŖĖŲµÄŹĒ_____£ØĢīŠņŗÅ£©£®
£Ø4£©Ķ¼CŗĶDĖłŹōŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ_____£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ®¹øÖ÷ŅŖ³É·ÖŹĒĢ¼ĖįøĘ”¢ĒāŃõ»ÆĆ¾¼°ÉŁĮæĖ®£¬ŹµŃéŹŅĻÖÓŠŅ»Ė®¹øѳʷ£¬ĪŖ²ā¶ØĘäÖŠø÷³É·ŻµÄÖŹĮæ·ÖŹż£¬Ä³ŠĖȤŠ”×éµÄĶ¬Ń§ĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃé£ØøĆ×°ÖĆĘųĆÜŠŌĮ¼ŗĆ£¬A”¢C”¢DÖŠĖł×°Ņ©Ę·×ćĮ棩”£
ŅŃÖŖ£ŗ¢Ł¼īŹÆ»ŅŹĒŃõ»ÆøĘŗĶĒāŃõ»ÆÄʵĻģŗĻĪļ£»
¢ŚøßĪĀĢõ¼žĻĀ£¬Ģ¼ĖįøĘ”¢ĒāŃõ»ÆĆ¾¾łŅ×·Ö½āĪŖĮ½ÖÖŃõ»ÆĪļ”£
²æ·ÖŹµŃé²½ÖčČēĻĀ£ŗ
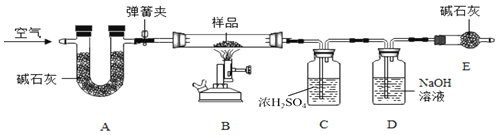
¢ń£®Č”8gѳʷװČė×°ÖĆBµÄ²£Į§¹ÜÖŠ£¬°“Ķ¼Į¬½ÓŗĆ×°ÖĆ£¬¹Ų±ÕµÆ»É¼Š£¬øųѳʷ¼ÓČČ£»
¢ņ£®“żŃłĘ·ĶźČ«·“Ó¦ŗó£¬______£ØĢī×ÖÄøŠņŗÅ£©£»
A ĻČ“ņæŖµÆ»É¼ŠĶØČėæÕĘų£¬ŌŁĻØĆš¾Ę¾«ÅēµĘ£¬Ö±µ½ĄäČ“£»
B ĻČĻØĆš¾Ę¾«ÅēµĘ£¬²£Į§¹ÜĄäČ“ŗóŌŁ“ņæŖµÆ»É¼ŠĶØČėæÕĘų
¢ó£®ŹµŃéĶź±Ļ£¬²āµĆ×°ÖĆC”¢DÖŠµÄŅŗĢåÖŹĮæ·Ö±šŌö¼ÓĮĖ1g”¢2.2g£»
¢ō£®øł¾ŻŹµŃéĖł²āŹż¾Ż¼ĘĖćøĆѳʷ֊Ģ¼ĖįøĘ”¢ĒāŃõ»ÆĆ¾µÄÖŹĮæ·ÖŹż”£Ēė»Ų“š£ŗ
£Ø1£©Š“³öĒāŃõ»ÆĆ¾·Ö½āµÄ·“Ó¦·½³ĢŹ½ĪŖ______”£
£Ø2£©·“Ó¦½įŹųŗó¹ÄČėæÕĘųµÄÄæµÄŹĒ______”£
£Ø3£©×°ÖĆBÖŠµÄ·“Ó¦·½³ĢŹ½______£¬______”£
£Ø4£©×°ÖĆCµÄ×÷ÓĆŹĒ______£¬DµÄ×÷ÓĆŹĒ______”£
£Ø5£©ĒóøĆĖ®¹øѳʷ֊Ģ¼ĖįøʵÄÖŹĮæ·ÖŹż”£______£ØŠ“³ö¼ĘĖć¹ż³Ģ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ£ŃóŌĢ²Ų×Å·įø»µÄ׏Ō“”£ĪŅ¹ś¹ś²śŗ½Äø001AŅŃ¾½Ø³ÉĻĀĖ®£¬¼“½«ŗ£ŹŌ”£Ėż½«ÓĆÓŚ±£»¤ĪŅ¹śŗ£Ńó¹śĶĮ°²Č«”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø””””£©

A. ŗ£Ńó·łŌĮÉĄ«£¬Ō¶ŗ£ŹĒĒćµ¹Ą¬»ų·ĻĪļµÄĄķĻė³”Ėł
B. ¹¤ŅµÉĻÓĆŗ£Ė®É¹ŃĪƻӊ°Ńŗ£Ė®É¹øÉ£¬ŌŅņŹĒ·ĄÖ¹ŗ£Ė®ÖŠĀČ»ÆĆ¾µČæÉČÜŠŌŌÓÖŹĖęĀČ»ÆÄĘŅ»Ęš½į¾§Īö³ö
C. ŗ£ŃóÖŠÓµÓŠ·įø»µÄÓęŅµ×ŹŌ“£¬æÉŅŌ“óĖĮ²¶ĄĢø÷ÖÖŗ£ĻŹ
D. æÉŅŌÓĆŗ£Ė®ĢįĮ¶½šŹōĆ¾ŹĒŅņĪŖŗ£Ė®ÖŠŗ¬ÓŠ½šŹōĆ¾
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»Æ¹¤ĘóŅµ·¢ÉśĮĖĒā·śĖįŠ¹Ā©ŹĀ¼ž£¬¾¹żĻū·Ą¹Ł±ųŗĶĻą¹Ų×ؼŅ¼°Ź±æĘѧµÄĻÖ³”“¦Ąķ£¬ŹĀ¹ŹµĆµ½ĮĖæŲÖĘ”£Ēā·śĖįŹĒ·ś»ÆĒāĘųĢåµÄĖ®ČÜŅŗ£¬³ŹĖįŠŌ£¬ĒŅÓŠ¾ē¶¾ŠŌŗĶøÆŹ“ŠŌ£¬Ęä¾ß±øĖįµÄĶØŠŌ”£µ±ÉŁĮæµÄĒā·śĖįŠ¹Ā©Ź±£¬æÉÓĆɳĶĮŗĶøÉŌļŹģŹÆ»ŅµÄ»ģŗĻĪļĄ“×öÓ¦¼±“¦Ąķ£¬ĘäÖŠ·“Ó¦µÄÓŠŠ§³É·ÖĪŖŹģŹÆ»ŅÖŠµÄĒāŃõ»ÆøĘ”£Ēėøł¾ŻŅŌÉĻŠÅĻ¢·ÖĪö»Ų“š£ŗ
£Ø1£©“ÓĪļÖŹ·ÖĄąµÄ½Ē¶ČĄ“æ“£¬Ēā·śĖįŗĶŹģŹÆ»Ņ¶¼ŹōÓŚ_____
£Ø2£©¼ŁÉčŹĀ¹ŹÖŠÓŠ35%µÄĒā·śĖį4tŠ¹Ā©£¬¼ĘĖćŌŚĄķĀŪÉĻŠčŅŖ¶ąÉŁĒāŃõ»ÆøĘĄ“×öĻÖ³”“¦Ąķ£æ_____
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŹµŃ銔×éÓūĢ½¾æŃĪĖį”¢ĒāŃõ»ÆøĘĮ½ÖÖĪļÖŹµÄ»ÆѧŠŌÖŹ£¬Č”8Ö§ŹŌ¹Ü·Ö±šÓĆA”«H±ąŗÅŗó£¬×öČēĻĀŹµŃ锣
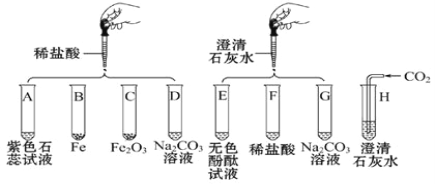
(1)ŹµŃéÖŠ¹Ū²ģµ½ÓŠĘųÅŻ³öĻֵďŌ¹ÜŹĒ_____£¬ÓŠ³ĮµķÉś³ÉµÄŹŌ¹ÜŹĒ_____”£
(2)Š“³öŹµŃéÖŠĪŽĆ÷ĻŌĻÖĻó²śÉśµÄŹŌ¹ÜÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½_____”£
(3)ŹµŃéŗóijŹŌ¹ÜÖŠĪŖŗģÉ«ČÜŅŗ£¬µ±ĻņĘäÖŠ¼ÓČė¹żĮæµÄ_____ŗó£¬ČÜŅŗ±äĪŖĪŽÉ«”£ÓÉ“ĖĶʶĻ£¬øĆŹŌ¹ÜÖŠ×ī³õŹ¢ÓŠµÄĪļÖŹŹĒ_____”£
(4)ŹµŃéŗóijŹŌ¹ÜµÄµ×²æÓŠ°×É«¹ĢĢ壬¹żĀĖŗóĻņĀĖŅŗÖŠµĪ¼ÓĻ”ŃĪĖį£¬Ņ»¶ĪŹ±¼äŗóÓŠĘųÅŻ³öĻÖ£¬ŌņøĆĀĖŅŗÖŠµÄČÜÖŹŹĒ_____”£
(5)ŹµŃéŗóijŹŌ¹ÜÖŠÖ»µĆµ½ĪŽÉ«ČÜŅŗ£¬ĻņĘäÖŠ¼ÓČė×ćĮæµÄNa2CO3ČÜŅŗ£¬ĪŽĆ÷ĻŌĻÖĻó”£ÓÉ“ĖĶʶĻ£¬øĆŹŌ¹ÜÖŠ×ī³õ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____£¬ŌĪŽÉ«ČÜŅŗÖŠµÄČÜÖŹŹĒ_____£ØŠ“³öĖłÓŠæÉÄÜ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潚Źō¼°Ę佚ŹōÖĘĘ·¶ŌČĖĄąÉē»įµÄ·¢Õ¹ÓŠ×ż«ĘäÖŲŅŖµÄ×÷ÓĆ”£
Ęū³µÖĘŌģ¹ż³ĢÖŠŅŖÓƵ½“óĮæµÄĢś”¢Ķ”¢ĀĮµČ½šŹō²ÄĮĻ£¬Ēė°“ŅŖĒóĢīæÕ”£
£Ø1£©Ęū³µÖĘŌģÖŠÓƵĆ×ī¶ąµÄ½šŹō²ÄĮĻŹĒøÖ”£øÖ____£ØĢī”°ŹĒ”±»ņ”°²»ŹĒ”±£©“潚Źō”£ĪŖĮĖ·ĄÖ¹³µĢå±ķĆęÉśŠā£¬³µĢåŅŖ½ųŠŠ____”£Į¶ĢśµÄŌĄķŹĒĄūÓĆŅ»Ńõ»ÆĢ¼ÓėŃõ»ÆĢś·“Ó¦»¹Ō³öĢś£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___________________”£
£Ø2£©Ęū³µµēĀ·ÖŠµÄµ¼Ļß“ó¶¼ŹĒĶŠ¾µÄ£¬ÕāÖ÷ŅŖŹĒĄūÓĆĮĖĶµÄ____ŠŌ”£½«³ąĶæó£ØÖ÷ŅŖ³É·ÖCu2O£©ŗĶ»ŌĶæó£ØÖ÷ŅŖ³É·ÖCu2S£©»ģŗĻ±ŗÉÕæɵƵ½Ķ£¬Ēė½«·“Ó¦µÄ·½³ĢŹ½²¹³äĶźÕū£ŗ2Cu2O+Cu2S![]() 6Cu+____”£
6Cu+____ӣ
£Ø3£©Ģś”¢Ķ”¢ĀĮČżÖÖŌŖĖŲŌŚµŲæĒÖŠµÄŗ¬Įæ×ī“óµÄŹĒ_______£¬µ«ČżÖÖ½šŹō±»ČĖĄą·¢ĻÖŗĶĄūÓƵď±¼äŹĒĶ×īŌē£¬¶ųĀĮ×īĶķ£¬Ö÷ŅŖŹĒŅņĪŖĀĮ¾ßÓŠŗÜŗƵÄæ¹øÆŹ“ŠŌÄÜ£¬ŌŅņŹĒ______£ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£©”£
£Ø4£©ĪŖĮĖĢ½¾æĀĮ”¢Ģś”¢ŅųČżÖÖ½šŹō»ī¶ÆŠŌĖ³Šņ£¬æÉŃ”ŌńAl”¢AgŗĶ____Ą“½ųŠŠŹµŃ锣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”沤²ĖÓŖŃų·įø»£¬ĖŲÓŠ”°Źß²ĖÖ®Ķõ”±µÄĆĄ³Ę£®Ćń¼äĮ÷“«£ŗ²¤²Ė¶¹øÆĶ¬Ź³£¬Ņ×µĆ½įŹÆ£®Ä³»ÆѧŠĖȤŠ”×é¶Ō”°²¤²Ė¶¹øÆŹĒ·ń²»ÄÜĶ¬Ź³”±µČĪŹĢā½ųŠŠĮĖĢ½¾æ£®
£Ø²éŌÄ׏ĮĻ£©¢Ł²¤²Ėŗ¬ÓŠ·įø»µÄĢś”¢²ŻĖįŃĪ”¢Ģ¼ĖįŃĪµČ£¬¶¹øÆÖŠŗ¬ÓŠ·įø»µÄµ°°×ÖŹ¼°øĘŃĪ£® ¢ŚČĖĢå½įŹÆµÄÖ÷ŅŖ³É·Ö£ŗ²ŻĖįøĘ£ØCaC2O4£© ¢Ū“×Ėį²»Óė²ŻĖįøĘ·“Ó¦£¬µ«ÄÜÓėĢ¼ĖįøĘ·“Ӧɜ³ÉæÉČÜŠŌŃĪµČ£®
£ØĢį³ö²ĀĻė£©”°²¤²Ė¶¹øƲ»ÄÜĶ¬Ź³”±µÄŌŅņæÉÄÜŹĒ£ŗ£Ø1£©_____
£ØĢ½¾æŅ»£©²¤²ĖÖŠ²æ·Ö³É·Ö·ÖĪö
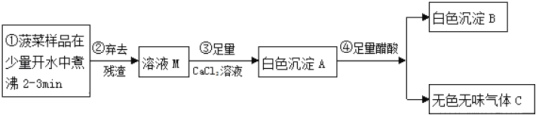
£Ø2£©²½Öč¢ŪÖŠ¼ÓČė×ćĮæµÄCaCl2ČÜŅŗµÄÄæµÄŹĒĢķ¼Ó_____Ąė×Ó£®
£Ø3£©ŅŃÖŖĘųĢåCÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬“×ĖįµÄ»ÆѧŹ½ÓĆHAC±ķŹ¾£¬Š“³ö²½Öč¢ÜµÄ»Æѧ·“Ó¦·½³ĢŹ½_____£®³ĮµķA”¢BµÄÖŹĮæ¹ŲĻµĪŖ£ŗm£ØA£©_____m£ØB£©£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©£®
£Ø4£©°×É«³ĮµķBµÄ»ÆѧŹ½ĪŖ_____£¬ÓÉ“Ėæɼū²¤²Ė¶¹øƲ»ÄÜĶ¬Ź³£®
£Ø5£©ŅŌĻĀŅūŹ³¹ŪµćÕżČ·µÄŹĒ_____£ØĢīŠņŗÅ£©
A ½ū³Ō²¤²Ė B øßøĘÅ£ÄĢæÉÓė²¤²ĖĶ¬Ź³C ²¤²ĖÅėāæŹ±æÉÓĆæŖĖ®ĢĢ£¬½µµĶ²ŻĖįŃĪŗ¬Į森
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com