
 请回答下列有关问题:
请回答下列有关问题:| 氯化钠的质量 |
| 溶液质量 |


科目:初中化学 来源: 题型:
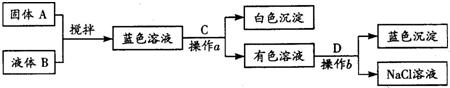
查看答案和解析>>
科目:初中化学 来源: 题型:
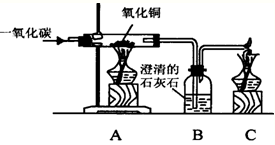 某同学使用如图所示装置,试验一氧化碳与氧化铜的反应.请回答下列有关问题:
某同学使用如图所示装置,试验一氧化碳与氧化铜的反应.请回答下列有关问题:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2012?哈尔滨一模)在学过酸碱能发生中和反应后,张南同学和小岗同学想用实验的方法来证明氢氧化钠能与硫酸能发生化学反应,请回答下列有关问题.
(2012?哈尔滨一模)在学过酸碱能发生中和反应后,张南同学和小岗同学想用实验的方法来证明氢氧化钠能与硫酸能发生化学反应,请回答下列有关问题.| 预计现象 | 解释与结论 | |
| 小岗同学 | 产生气泡 | 加入碳酸钠溶液后.产生气泡.说明硫酸还存在,没有和氢氧化钠发生化学反应. |
| 张南同学 | 没有产生气泡 | 加入碳酸钠溶液后,没有产生气泡.说明硫酸不存在,和氢氧化钠发生了化学反应. |
查看答案和解析>>
科目:初中化学 来源: 题型:

 ”表示氯原子,“
”表示氯原子,“ ”表示钠原子,“
”表示钠原子,“ ”表示氧原子)该反应的化学方程式为
”表示氧原子)该反应的化学方程式为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com