
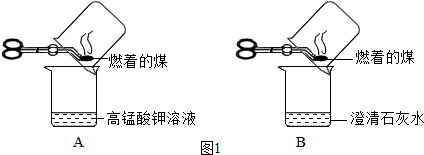
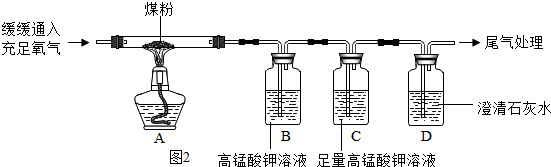
分析 【查阅资料】:①根据质量守恒定律,反应前后原子个数不变可解答;②根据二氧化碳与澄清石灰水反应生成碳酸钙和水解答;
交流讨论】:根据质量守恒定律,前后元素种类不变,可解答;根据二氧化硫也能使石灰水变浑浊来解答;根据二氧化碳和二氧化硫的化学性质来解答;
【实验反思】:(1)根据使反应充分的条件解答;
(2)实验中C装置的作用是检验二氧化硫是否存在;
解答 解:【查阅资料】:①根据质量守恒定律,反应前后原子个数不变,5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2X,可推出X的化学式为H2SO4;
②二氧化碳与澄清石灰水反应生成碳酸钙和水,反应的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O.
【交流讨论】:(1)根据质量守恒定律,前后元素种类不变,煤燃烧时即生成了二氧化碳和二氧化硫,所以可推断煤中必含有碳元素和硫元素;
(2)乙质疑甲同学的方案的合理性,其质疑的理由是二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,所以B变浑浊不能确定是否生成了二氧化碳;
(3)实验现象B中的高锰酸钾溶液褪色说明生成了二氧化硫,D中的澄清石灰水变浑浊说明有二氧化碳生成,由质量守恒定律可证明煤中含有碳元素和硫元素;
【实验反思】:(1)将煤块粉碎成煤粉的目的是使煤充分反应或完全反应;
(2)实验中C装置的作用是检验二氧化硫是否存在.
答案:
【查阅资料】:①H2SO4;②CO2+Ca(OH)2=CaCO3↓+H2O.
【交流讨论】:(1)煤燃烧时生成了二氧化碳和二氧化硫;
(2)二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,B变浑浊不能确定是否生成了二氧化碳;
(3)B中的高锰酸钾溶液褪色,D中的澄清石灰水变浑浊
【实验反思】:
(1)使煤充分反应;
(2)应该是除去二氧化硫并检验二氧化硫是否除尽.
点评 本题主要考查二氧化硫和二氧化碳的性质区别与联系,还有质量守恒定律的应用,锻炼了学生的综合分析解决问题的能力,和应变拓展能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
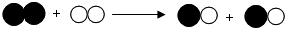 图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,你认为下列说法正确的是( )
图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,你认为下列说法正确的是( )| A. | 该反应中各元素的化合价均发生了改变 | |
| B. | 该反应既不是化合反应,也不是分解反应 | |
| C. | 该反应中的所有物质都是由原子构成的 | |
| D. | 反应中分子的种类和原子的种类均没有改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气的主要成分是氮气和氧气 | B. | CO2的大量排放会造成温室效应 | ||
| C. | 氦气可用来填充探空气球 | D. | 室内起火时要打开所有门窗通风 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 三氯生中含有氧分子 | |
| B. | 三氯生由碳、氢、氯、氧四种元素组成 | |
| C. | 三氯生是一种含氧化合物 | |
| D. | 三氯生分子中含有25个原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 猜想 | 可行的实验方案 | 实验现象 |
| 猜想1 | 将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象. | 果肉表面不变色. |
| 猜想2 | 将一小块切开的苹果放入盛有氮气的集气瓶中,观察现象. | 果肉表面不变色. |
| 猜想3 | 将切开的苹果放入盛有氧气的集气瓶中,观察现象. | 果肉表面变色. |
| 猜想4 | 果肉表面不变色. | |
| 猜想⑤ | 温度高的先变色. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com