
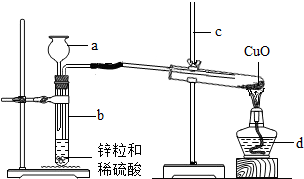
 如图是某同学设计的实验室制取氢气,并用氢气还原氧化铜的实验装置,根据图回答下列问题.
如图是某同学设计的实验室制取氢气,并用氢气还原氧化铜的实验装置,根据图回答下列问题.

科目:初中化学 来源: 题型:阅读理解

| 验实号编 | 试剂 | 前 10min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30mL 30% | 564.3 |
| b | 含杂质的锌 | 30mL 30% | 634.7 |
| c | 纯锌 | 30mL 20% | 449.3 |
| d | 纯锌 | 40mL 30% | 602.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
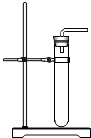 (2012?安徽模拟)同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如图).该反应的化学方程式为
(2012?安徽模拟)同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如图).该反应的化学方程式为
| ||
| ||
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 另一名同学的猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 细铁丝在氧气中燃烧会火星四射,某兴趣小组对其产生原因进行探究.
细铁丝在氧气中燃烧会火星四射,某兴趣小组对其产生原因进行探究.| 铁 丝 材 质 | 实 验 现 象 |
| 纯铁丝 | 火星很少,燃烧不剧烈 |
| 低碳钢丝 | 火星较多,燃烧剧烈 |
| 高碳钢丝 | 火星四射,燃烧剧烈 |
| ||
| ||
| ||
| ||
| 铁丝根数 | 铁丝燃烧情况 |
| 1根细铁丝 | 燃烧不剧烈,有火星四射. |
| 2根细铁丝拧成一束 | 比1根铁丝燃烧剧烈,火星四射明显. |
| 3根细铁丝拧成一束 | 比2根铁丝燃烧剧烈,火星四射更明显. |
查看答案和解析>>
科目:初中化学 来源: 题型:
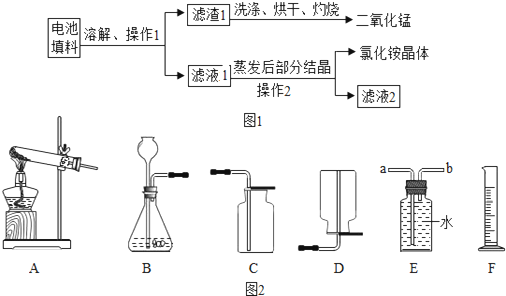
| 验实号编 | 试 剂 | 前 10min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30mL 30% | 564.3 |
| b | 含杂质的锌 | 30mL 30% | 634.7 |
| c | 纯锌 | 30mL 20% | 449.3 |
| d | 纯锌 | 40mL 30% | 602.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
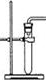 同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如图).该反应的化学方程式为________.某小组甲、乙、丙三名同学用该装置进行实验过程中,橡皮塞突然被弹飞,并有少量的液体溅到实验台和衣服上.就此异常现象这三名同学进行了如下探究:
同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如图).该反应的化学方程式为________.某小组甲、乙、丙三名同学用该装置进行实验过程中,橡皮塞突然被弹飞,并有少量的液体溅到实验台和衣服上.就此异常现象这三名同学进行了如下探究:| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 另一名同学的猜想正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com