
【题目】某品牌碳酸氢铵化肥的标签如图所示。根据相关信息判断下列计算正确的是

A.碳酸氢铵中氮、氢、氧、碳四种元素的质量比14:4:48:12
B.碳酸氢铵中各元素的质量分数由大到小的顺序为O、C、H、N
C.该化肥中碳酸氢铵的纯度为79%
D.每袋该化肥中含氮量与30kg尿素[化学式为CO(NH2)2]含氮量相当
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下图中A、B、C、D是四种粒子的结构示意图。
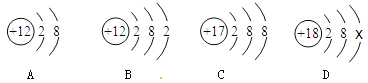
请回答下列问题:
(1)图中A、B、C、D属于_______种元素的粒子;
(2)A、B、C、D四种粒子中,不具备稳定结构的是_________(填序号);
(3)D中x=________;
(4)A与C形成化合物的化学式是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案不能达到目的是( )
A.探究铁生锈是否与氧气有关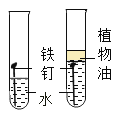
B.探究Fe、Cu、Ag金属活动性顺序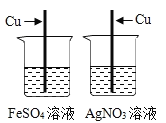
C.测定空气中氧气含量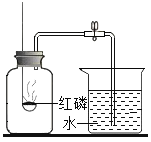
D.探究可燃物燃烧是否需要氧气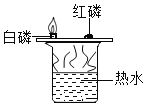
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以太阳能为热源经由铁氧化合物循环分解水的过程如图所示。下列说法错误的是( )
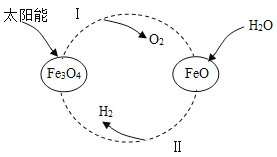
A.过程中,铁、氢、氧元素的化合价都发生了变化
B.该过程实现了太阳能向化学能的转化
C.过程I的化学方程式为 2Fe3O4 6FeO+O2↑
6FeO+O2↑
D.过程II属于置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
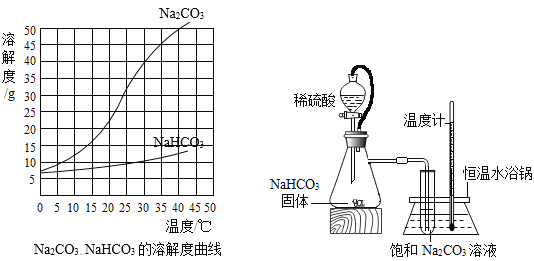
【题目】由于溶解度不同(如图所示),饱和碳酸钠溶液中通入CO 2会析出碳酸氢钠晶体而使溶液变浑浊。某化学课外小组同学发现不同条件下出现浑浊的时间不同。
(提出问题)影响碳酸氢钠晶体产生速率的因素有哪些?
(猜想与假设)碳酸氢钠晶体产生速率的影响因素有温度、试管内径、CO2流速、饱和碳酸钠溶液的体积。
(进行实验)实验装置如图所示。每次实验时均在试管里加入1mL饱和碳酸钠溶液并在试管后放置一张写有黑色字迹的白纸,从垂直于试管的方向观察白纸上字迹的清晰程度,记录时间,用于判断碳酸氢钠晶体的产生速率。部分实验记录如下表所示:
序号 | 温度(℃) | 试管内经(mm) | CO2流速 (个气泡/s) | 产生不同现象的时间(s) | ||
字迹变浅 | 字迹模糊 | 字迹消失 | ||||
① | 25 | 10 | 5~8 | 517" | 719" | 817" |
② | 32 | 10 | 5~8 | 350" | 409" | 428" |
③ | 40 | 10 | 5~8 | 348" | 406" | 418" |
④ | 25 | 14 | 5~8 | 636" | 738" | 828" |
⑤ | 25 | 25 | 5~8 | X | 943" | 1022" |
⑥ | 25 | 10 | 10~13 | 502" | 640" | 758" |
⑦ | 25 | 10 | 2~5 | 540" | 1045" | 1236" |
(解释与结论)
(1)由上述溶解度曲线图可知溶解度受温度影响相对更大的物质是_________________。
(2)锥形瓶中是利用碳酸氢钠与稀硫酸反应来制取二氧化碳。除生成二氧化碳外,还有水和硫酸钠生成,该反应的化学方程式为_____________________。
(3) 同学们若要研究饱和碳酸钠溶液的体积对碳酸氢钠晶体产生速率是否有影响,需要控制的变量有__________________。
(4)由实验①②③,可得出的结论是____________________。
(5)实验①④⑤研究的影响因素是___________________。
(6)通过对数据的观察和分析,小倩认为“二氧化碳流速越快,碳酸氢钠晶体产生速率越快”,得到该结论的依据是______________(填实验序号)。
(反思与评价)
(7)表中X的取值范围应该是_______________。
(8)该实验采用硫酸而不是盐酸来制备二氧化碳的原因是__________________。
(9)如图中使用橡皮管连接分液漏斗与锥形瓶的目的是__________________。
(10)如何除去碳酸钠中混有的少量碳酸氢钠?___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸锂广泛应用于陶瓷和医药等领域。以β-锂辉石(主要成分为Li2O·Al2O3·4SiO2)为原料制备Li2CO3的工艺流程如下:
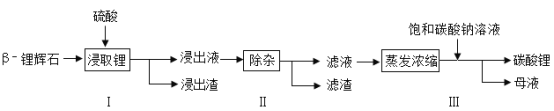
已知:Fe3 +、Al3 +、Fe2 +和Mg2 +以氢氧化物形式完全沉淀时,溶液的pH分别为 3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在30℃下的溶解度分别为34.2 g、12.7 g和1.3g。
(1)步骤I前,β-锂辉石要粉碎成细颗粒的目的是__________________。
(2)步骤I中,酸浸后得到的酸性溶液除含有Li+、SO42-,还含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_________(填“石灰石”、 “氯化钙”或“稀硫酸”)以调节溶液的pH到6.0~6.5,使Al3+、Fe3+形成沉淀,然后分离得到浸出液。
(3)步骤II中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有_______________________。
(4)从母液中可回收的主要物质是__________________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制取气体时常用的部分仪器,回答问题。
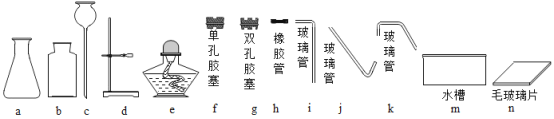
(1)用高锰酸钾制取氧气:
①写出该反应的化学方程式_________;
②检验收集到的![]() 方法是___________。
方法是___________。
(2)用大理石和盐酸反应制取![]() 并用向上排空气法收集
并用向上排空气法收集
①组装制取装置时,需选择上图中的a、b、g、h、i、j、n和________;
②计算制取4.4g二氧化碳,至少需用________g质量分数为10%的稀盐酸和足量的大理石反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如图所示。试计算:
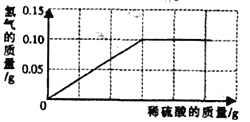
(1)样品中铜的质量分数;
(2)反应所消耗的硫酸溶液质量;
(3)反应后所得溶液质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列除杂方法(括号内为杂质)中正确的是( )
A.二氧化碳(一氧化碳):通入氧气,点燃
B.硝酸铜溶液(硝酸银):加入足量的铜粉,过滤
C.碳酸钙固体(氯化钙):加入足量的水溶解,过滤、洗涤、干燥
D.![]() 溶液(
溶液(![]() ):加入适量的氯化钡溶液、过滤
):加入适量的氯化钡溶液、过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com