
【题目】南海是我国的固有领海,蕴含着丰富的海洋资源,2017年5月18日,我国南海神狐海域的可燃冰试采取得到圆满成功,实现历史性突破。

(1)可燃冰的主要成分是甲烷,试写出甲烷在空气中燃烧的化学方程式_____。
(2)可燃冰被科学家誉为“未来能源”“21世纪能源”,原因是_____。
(3)1926年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展.侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠.Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:
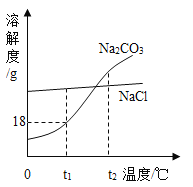
①t1℃时,NaCl的溶解度_____ Na2CO3的溶解度(填“大于”“等于”或“小于”之一);
②t1℃时,50g水中加入10gNa2CO3,经充分溶解,所得溶液中溶质与溶液的质量之比为_____(填最简整数比);
③t1℃时,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温到t2℃,此时所得碳酸钠溶液溶质质量分数_____ 氯化钠溶液溶质质量分数(填“大于”“等于”或“小于”或“无法判断”之一)。
【答案】![]() 可燃冰储量大,甲烷燃烧无污染 大于 9:59 小于
可燃冰储量大,甲烷燃烧无污染 大于 9:59 小于
【解析】
(1)可燃冰的主要成分是甲烷,甲烷在空气中燃烧的化学方程式![]() 。
。
(2)可燃冰被科学家誉为“未来能源”“21世纪能源”,原因是可燃冰储量大,甲烷燃烧无污染。
(3)①根据曲线图分析,在t1℃时,NaCl的溶解度大于Na2CO3的溶解度。
②在t1℃时,Na2CO3的溶解度为18g ,那么50g水中最多能溶解9gNa2CO3,所得溶液中溶质与溶液的质量之比为9:59。
③在t1℃时,已知碳酸钠的溶解度小于氯化钠的溶解度,那么碳酸钠饱和溶液的溶质质量分数小于氯化钠饱和溶液的溶质质量分数,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温到t2℃,两溶液中的溶质质量和溶剂质量都不变,溶质的质量分数也不变,与t1℃时的相同,所以所得碳酸钠溶液溶质质量分数小于氯化钠溶液溶质质量分数。


科目:初中化学 来源: 题型:
【题目】下列是有关碳酸钠与盐酸反应的实验及图像,有关说法错误的是
A.实验甲不能用于验证质量守恒定律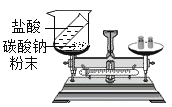
B.实验乙能用于在实验室制取二氧化碳
C.实验丙中澄清石灰水未变浑浊,可能因为盐酸太浓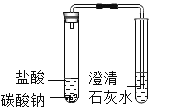
D.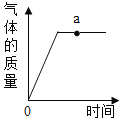 图像丁中a点所对应溶液中的阴离子可能是Cl-和CO32-
图像丁中a点所对应溶液中的阴离子可能是Cl-和CO32-
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:
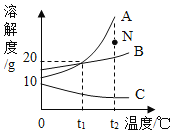
(1)N点对应的是物质A的____(填“ 饱和”或“不饱和”)溶液。
(2)加热C的饱和溶液,出现浑浊现象,其原因是____________。
(3)t1°C时,将A、B、C各8g分别加入盛有50g水的烧杯中,充分溶解,测得三种溶液中溶质的质量分数分别为w(A)、w(B)、w(C),则三者之间的大小关系是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学来源于生活,化学与生活密切相关。
(1)“合理膳食,均衡营养”会让我们更健康,下列食品中富含糖类的是__(填字母序号,下同)。
a 鸡蛋 b 馒头 c 蔬菜 d 花生油 e 米饭
(2)为了预防佝偻病,幼儿及青少年可以补充一些含_元素(填名称)的食品。
(3)铝块能制成铝箔是利用了铝的____性,铝的“白我保护”原因是___(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】课本第二单元课后作业中有“寻找新的催化剂”的探究内容,实验中学探究小组据此设计了如下探究方案。
[提出问题]红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
[实验探究]
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是_ ②___ |
II.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的__在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡且 __ | 红砖粉末的催化效果没有二氧化锰粉末好 |
[拓展应用]
己知CuSO4也可作为过氧化氢分解的催化剂。向101g 一定溶质质量分数的过氧化氢溶液中加入2gCuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气__g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列微观变化示意图回答问题。
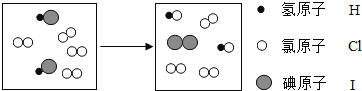
(1)反应物中碘元素的化合价为______________________。
(2)上图微观变化表示的反应属于四种基本反应类型中的_______________________反应。
(3)根据上面的微观变化图,请你总结出化学变化的实质是______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学会从微观角度看物质世界,是学习化学必须的要素,如图是某反应的微观示意图,下列说法正确的是(____)
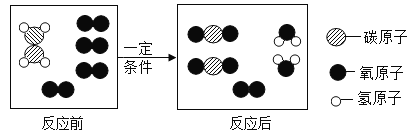
A 该反应属于置换反应
B 该反应前后分子总数减少了
C 该反应的生成物都是氧化物
D 参加反应的单质与化合物的分子个数比为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是一些初中化学常用物质的转化关系,其中 A 是含有两种元素的黑色固体,且 A 与 C 中含有某种相同元素,B、C、E、F 均是一种无色、无味的气体,J 是食品干燥剂,G的溶液为浅绿色。回答:

(1)G 所属物质的类别_______(选填“单质”、“氧化物”、“酸”、“碱”、“盐”)。
(2)写出反应⑤的化学方程式_____________________________ 。
(3)B 的一条用途_____。E的水溶液加热时 pH 值_____(填“变大”“不变”或“变小”)。
(4)写出反应③的实验现象_______;反应后溶液质量________(填“变大” “不变”或“变小”)。
(5)①—⑤反应中不包含的基本反应类型是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】久置的铜制品表面能生成绿色的铜锈[主要成分为Cu2(OH)2CO3],某化学兴趣小组对铜生锈的条件进行了以下探究。
(提出猜想)根据铜锈的组成元素推测,铜生锈可能是铜与空气中的二氧化碳、水等物质反应的结果。
(实验设计)兴趣小组同学取打磨光量的铜丝,设计了如图所示的四个实验。

(现象分析)若干天后,发现只有D瓶中的铜丝出现绿色的铜锈,其他瓶中的铜丝均无铜锈出现。
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是_____。
(2)B瓶与D瓶中的现象对比,可以得出的结论是_____。
(实验结论)由上述四个实验可分析得出,铜生锈是铜与空气中的_____共同作用的结果。
(拓展探究)以锈蚀严重的废铜屑为原料,回收制取纯铜。查阅资料:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑;Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑。如图是该兴趣小组设计的两种回收铜的实验方案:
2CuO+H2O+CO2↑。如图是该兴趣小组设计的两种回收铜的实验方案:

(分析评价)
(3)步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是_____,该操作中玻璃棒的作用是_____。
(4)步骤Ⅱ过程发生反应的化学方程式为_____,此实验开始时要先通一段时间CO再加热,目的是_____。
(5)同一份废铜屑分别通过上述两种方案最终得到的铜的质量:方案一:_____(填“>”或“=”或“<”)方案二:以上两种方案中,方案二优越于方案一,理由是_____(任答一点)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com