
(6��)�������������������Ӧ��ʮ�ֹ㷺��
(1)��ͼA�ǽ�����һ��Ӧ��ʵ���������ý�������Ҫ������____����ͼB���������Ƭ��̻����ڴ�ͭƬ�������ԵĻ��ۡ��ɴ˿ɵõ��Ľ�����____��

(2)д����ҵ����һ����̼�������ұ�������Ļ�ѧ����ʽ_________________________��
(3)ij��ȤС��ͬѧ���Ӻ������ᡢ��������������ͭ�ķ�Һ�л���ȫ����ͭ�����õ�����Ʒ�������������������ͼ��ʾ��
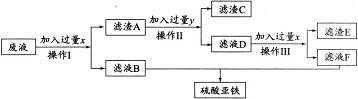
����� ��____��д�������йط�Ӧ�Ļ�ѧ����ʽ______________��
��____��д�������йط�Ӧ�Ļ�ѧ����ʽ______________��
��1�������� ��ͭ�ȴ�ͭ��Ӳ�ȴ�
��2��Fe2O3 + 3CO 2Fe + 3CO2
2Fe + 3CO2
��3��ϡ���ᣨ��H2SO4��
Fe + H2SO4=FeSO4 + H2�� Fe + CuSO4=FeSO4 + Cu (2��) д��1������ʽ��1��
��������
�����������1�������������ý����ĵ����ԣ�ͼB�������Ƭ��̻����ڴ�ͭƬ�������ԵĻ��ۣ�˵����ͭ�ȴ�ͭ��Ӳ�ȴ�
��2����ҵ����һ����̼�������ұ�������Ļ�ѧ����ʽΪFe2O3 + 3CO 2Fe + 3CO2
2Fe + 3CO2
��3����Ϊ���Ļ��ǿ��ͭ��ǿ���⣬�������ȼ�����������ۣ���Ӧ��ɺ���ˣ������к���ͭ��ʣ������ۣ�Ϊ�˳�ȥ���ۣ��õ�ͭ����Ҫ�������м��������ϡ���ᣬ�������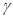 ��ϡ����йط�Ӧ�Ļ�ѧ����ʽΪFe + H2SO4=FeSO4 + H2�� ��Fe + CuSO4=FeSO4
+ Cu
��ϡ����йط�Ӧ�Ļ�ѧ����ʽΪFe + H2SO4=FeSO4 + H2�� ��Fe + CuSO4=FeSO4
+ Cu
���㣺���������ʣ��Ͻ�����ʣ���ѧ����ʽ���������˳���ӡ�
�������������˳��K��Ca��Na��Mg��Al��Zn��Fe��Sn��Pb����H����Cu��Hg��Ag��Pt��Au���ڽ������˳���У���ǰ�Ľ��������ᷢ���û���Ӧ����λ��Խ��ǰ����ӦԽ���ң�λ����ǰ�Ľ����ܰ�λ�����Ľ�����������Һ���û�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ���ݵ������꼶��һѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��30�֣�������Ի�ѧ��
��1�������е�ȼ��
���Ż��Ƚϣ�����ú Сľ�������������������=��������ú¯�����У������������Ŀ���� ��ú����ȫȼ�ղ���һ���ж�����Ļ�ѧʽ�� ��
����ˮ����ԭ���� ������ˮ��Ĥ��ĭ���������������ʱ��������Һ�����ĭ����������չ�γ�һ��ˮĤ���������ԭ���� ��
��2����������������;�㷺
������������Ʒ����Ҫ���ɽ��������Ƴɵ��� ��

�����������ʳ��ʱ������������м��θ��ת��Ϊ�ɱ����յ�Fe2+����Ӧ�Ļ�ѧ����ʽΪ ���� ��Ӧ���������Ӧ���ͣ���
����������װҩ���Ҫ���������� �ԣ�
��ͭ���кܺõ� �ԣ��ʿ������ߡ�����ʪ��ұ���������ָ ���ѧ����ʽ����ͭ�Ϳ����е�O2��H2O�� ������ͭ���Cu2(OH)2CO3�ݣ���Ӧ�Ļ�ѧ����ʽ�� ��
��3�������е�ˮ����Һ
�ٴ�����Ȼˮʱ�����õĻ������� �������ƣ�������������һ�����͵����������仯ѧʽΪ ��
��������500mL 0.9%��������ˮ���ܶ�Ϊ1.0 g/mL������ҪNaCl������Ϊ g�����ƹ����У��������������� ������NaClʱ����������������̣�1 g���������룩��������������ȷ����������Һ���������������� 0.9%�����������������=����
����ͼ�Ǿ�����ˮ�ļ���װ�ã�����˵����ȷ���� ��

A���������ˮ�Ǵ����� B����װ���ܶ�ˮɱ������
C����װ���ܰ�Ӳˮ��Ϊ��ˮ D������̿������ˮ�е�ɫ�ؼ���ζ
��KNO3������������������Ӫ��Һ���±��ṩ��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ�
|
�¶�/�� |
0 |
20 |
40 |
60 |
80 |
|
�ܽ��/g |
13.3 |
31.6 |
63.9 |
110 |
169 |
a�����ϱ����ܽ��KNO3���ܽ�����¶ȱ仯�������� ��
b��20��ʱ����20gKNO3����50gˮ�г���ܽ⣬������Һ������Ϊ g��
c������60��ʱ��KNO3������Һ210 g��������20�棬������KNO3 g��
��4��ʳƷ��װѧ�ʴ�
�������ز�����˻�����������հ�װ���ӳ���ʳƷ�ı����ڣ�ԭ���� ��
�ڽ�N2�����װ������������������ΪN2�Ļ�ѧ���� ������á����ȶ�������
����ͼ�ǡ�504˫�������ı�ǩ�����ʴ��������⣺

a���������ٺ��� �ֵ��ʣ�
b��ȡ����˫������������ˮ�У����ã�����ϲ���Һ��pH=9������pH��ֽ�ⶨ����������� ��ͨ��CO2���ϲ���Һ����ǣ�д�������仯�Ļ�ѧ����ʽ �� ��
c��Ϊ�ⶨ��˫������ʹ��Ч����ȡ����˫������������ͼ��ʾ��ʵ�飬һ��ʱ������Թ���ˮ����� 21%�����������������=������������ ��
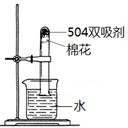
d������ʧЧ��˫�����У��к���ɫ���壬����Ҫ�� ��
e����˫�����У�NaCl�����ÿ����� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com