
【题目】有关下图中甲、乙、丙、丁所示实验的说法错误的是
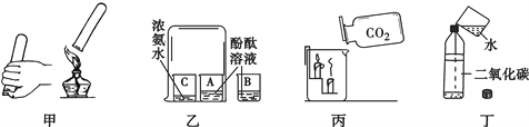
A.甲实验的目的是检验氢气的纯度,如果听到尖锐的爆鸣声, 则氢气不纯
B.乙实验说明分子是不断运动的
C.丙实验可证明通常情况下二氧化碳的密度比空气大且二氧化碳不能燃烧也不支持燃烧
D.丁实验既可证明二氧化碳能溶于水也可证明二氧化碳能与水反应
科目:初中化学 来源: 题型:
【题目】室温下,在pH=1的溶液中可大量共存的是
A. K+、Cl﹣、SO42﹣、OH﹣ B. Na+、SO42﹣、NO3﹣、CO32﹣
C. Ba2+、NO3﹣、Cl﹣、SO42﹣ D. NH4+、Cl﹣、NO3﹣、SO42﹣
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草酸与碳酸有相似的化学性质,在受热的条件下草酸也会分解。请你参与下列对草酸分解产物的实验探究过程。
【查阅资料】
草酸化学式为:H2C2O4;白色的无水硫酸铜遇水蒸气会变蓝色。
【提出猜想】
猜想一:草酸分解产物为CO2和H2O;猜想二:草酸分解产物是CO2、CO和H2O;
猜想三:草酸分解产物为CO2、H2和NO。
(1)甲同学认为,猜想三一定不成立,你认为其理由是 。
【实验验证】
乙同学设计下列由A~D四部分组成的装置验证猜想二。
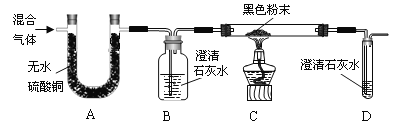
(2)实验时装置A中无水硫酸铜由白色变成蓝色,由此得到的结论是 。
(3)澄清石灰水中含有溶质的化学式是 ;能证明草酸分解混合气体中有CO2 产生的实验装置是________(填:“A”或“B”…),实验现象是 ;若装置C中黑色粉末变成红色,则发生反应的化学方程式是 。
【结论】
(4)若通过实验现象证明猜想二是正确的,则草酸分解的反应方程式是 。
【反思与评价】
(5)从环保角度分析,上述实验装置存在明显不足之处,你认为应该如何改进? 答: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质的学名、俗称与化学式表示同一种物质的是( )
A. 乙醇 酒精 CH3COOH B. 氧化钙 熟石灰 CaO
C. 氢氧化钠 烧碱 NaOH D. 汞 水银 Ag
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】晓蒙同学在做蜡烛燃烧的探究实验时发现,在蜡烛刚 熄灭时总会有一缕白烟冒出,
【提出问题】“白烟”的成分是什么呢?
【查阅资料】蜡烛是由石蜡和棉线烛芯组成的。蜡烛完全燃烧生成物为二氧化碳和水;蜡烛点燃时,灯芯周围的石蜡先熔化,从固态变为液态,一部分熔化的石蜡汽化为石蜡蒸气。石蜡蒸气燃烧产生火焰。
【猜 想】根据观察到的现象和资料,晓蒙同学提出如下3种猜想
A. “白烟”可能是蜡烛燃烧时生成的二氧化碳气体;
B. “白烟”可能是蜡烛燃烧时生成的水蒸气;
C. “白烟”可能是石蜡蒸气凝结成的石蜡固体小颗粒。
【实验验证】(1)吹灭蜡烛,并立即用一个内壁涂有澄清石灰水的烧杯罩住“白烟”,其目的是为了验证假设 (填序号),原因是
(2)吹灭蜡烛,并立即用一个干而冷的烧杯罩住“白烟”,烧杯内壁没有出现水雾,说明白烟不是 。
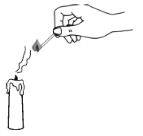
(3)吹灭蜡烛,并立即用燃着的木条去点“白烟”(如图所示)。发现蜡烛重新被点燃,说明“白烟”有可燃性,为假设 提供了证据。同时可排除假设 ,因为
(4)根据蜡烛完全燃烧的产物推出蜡烛的组成中一定有 元素、 元素可能有 元素。
(5)蜡烛燃烧过程中发生的变化是
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用的制取气体的发生装置如下:
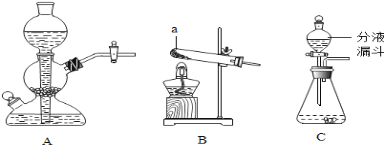
(1)搭建B装置时,酒精灯应在固定仪器a之 (选填(“前” 或“后”)放置,实验结束时应
(2)在实验室制取二氧化碳的研究中,进行了如下实验:
试验编号药品 | 甲 | 乙 | 丙 | 丁 |
大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
Ⅰ.上述实验中反应的化学方程式是 .
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验乙与 对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应快慢的因素是 .
(3)Ⅰ.研究发现酸浓度越大,产生气体的速度越快;浓盐酸有挥发性。与甲比较,对丁分析正确的是 (选填编号)
a.反应更为剧烈 b.最终反应装置中剩余物质的质量更小
c.产生二氧化碳的质量更大 d.粉末状大理石利用率更高
Ⅱ.下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因。
目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
制取二氧化碳 | 块状大理石 稀盐酸 | A | |
制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | C |
查看答案和解析>>
科目:初中化学 来源: 题型:
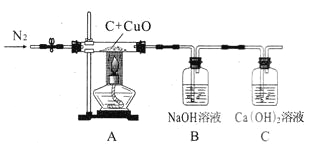
【题目】某化学小组利用下图所示的装置探究木炭粉和氧化铜反应后气体产物的成分。已知,该装置气密性良好;反应前木炭粉和氧化铜的质量为12.80g,玻璃管质量为52.30g;反应后玻璃管及其剩余固体的总质量为64.81g,装置B增重0.22g,装置C质量未改变。关于该实验,有下列说法:(C-12O-16)
①当玻璃管中有红色物质生成时,碳与氧化铜的反应结束
②玻璃管中反应结束后仍要缓缓通入氮气将装置内残留的气体生成物排出
③玻璃管中反应生成的气体只有二氧化碳
④NaOH与CO2反应导致装置B质量增加
⑤装置C的质量未改变说明没有气体通入该装置
以上说法正确的个数是
A.1个
B.2
C.3个
D.4个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com