
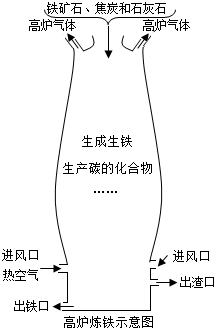
 如图所示的炼铁高炉中发生了许多化学反应,其中就涉及到碳及其化合物的相互转化.请回答下列问题.
如图所示的炼铁高炉中发生了许多化学反应,其中就涉及到碳及其化合物的相互转化.请回答下列问题.分析 (1)根据碳完全燃烧的产物下化学方程式;
(2)根据二氧化碳与炽热碳的反应解答;
(3)在反应中,氧化铁失去了氧,发生了还原反应,是氧化剂.一氧化碳得到了氧,发生了氧化反应,是还原剂;
(4)利用赤铁矿石的质量与赤铁矿石中氧化铁的质量分数和生铁中铁的质量分数,根据氧化铁与一氧化碳反应的化学方程式,可以计算出生铁的质量.
解答 解:(1)焦炭充分反应生成二氧化碳,化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2;故填:O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)炼铁高炉内焦炭与二氧化碳反应生成一氧化碳,反应的化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;故填:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(3)生成生铁的主要反应为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,由反应式可知,氧化铁在反应中失去了氧,发生了还原反应,是氧化剂,一氧化碳在反应中得到氧是还原剂;
故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B;
(4)解:设日产含Fe98%的生铁的质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
4900t×76% x×98%
$\frac{160}{112}=\frac{4900t×76%}{x×98%}$
解得:x=2660t
答:该厂理论上可日产含Fe98%的生铁的质量是2660t.
故填:2660.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.


科目:初中化学 来源: 题型:解答题
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
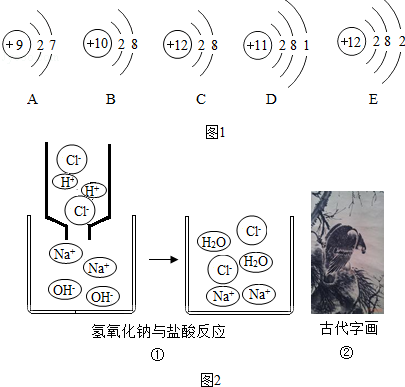
| A. | 水由氢原子和氧原子构成 | B. | 水由氢元素和氧元素构成 | ||
| C. | 水中氢、氧元素的个数比为2:1 | D. | 水中氢、氧元素的质量比比2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 常见的复合肥料有硝酸钾(KNO3)、磷酸二氢铵(NH4H2PO4)等 | |
| B. | 应将硫酸铵和熟石灰混施,在给作物提供氮元素的同时,又能降低土壤的酸性 | |
| C. | 若将农家肥和化肥综合施用,有助于提高化肥的增产效益 | |
| D. | 化肥使用不合理时,土壤结构会遭到破坏,还会因流失而污染江河湖泊 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
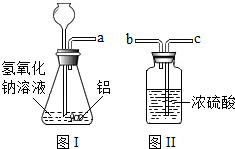 实验中,小红误将氢氧化钠溶液当成酸滴加到金属铝中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了以下探究
实验中,小红误将氢氧化钠溶液当成酸滴加到金属铝中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了以下探究查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可用纯碱与石灰水制烧碱 | B. | 它们易溶于水 | ||
| C. | 它们都是烹调调味品 | D. | 它们加酸都能放出二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
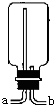 实验室开放日,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体”之间的反应进行一些探究.
实验室开放日,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体”之间的反应进行一些探究.| 实验步骤 | 实验现象 | 实验结论 |
| 将气体通入澄清石灰水中 | 澄清的石灰水变浑浊 | 证明该气体是二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com