
亚硝酸钠有良好的防腐作用,常用做肉类食品的添加剂。亚硝酸钠呈碱性,容易被误食,过量食用会中毒,因而用量严格限制。
亚硝酸钠易溶于水,其水溶液呈碱性,暴露在空气中易与氧气反应生成硝酸钠,加热至220 ℃以上会分解出红棕色、有刺激性气味、有毒的气体。
请根据以上信息回答:
(1)亚硝酸钠的保存方法是__________________;
(2)区分亚硝酸钠和食盐的方法是_____________________________________________________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
将一定量的xFeSO4·y(NH4)2·6H2O晶体加入到过量的NaOH溶液中,加热生成NH3 0.85g(假设生成的NH3全部逸出),过滤、洗涤、灼烧,得Fe2O3固体2.0g,则x、y的关系正确的是( )
A.x∶y=1∶1 B.x∶y=1∶2 C.x∶y=1∶4 D.x∶y=2∶1
查看答案和解析>>
科目:初中化学 来源: 题型:
“黄铜”是铜、锌合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下:(烧杯质量均为56 g)
| 甲 | 乙 | 丙 | |
| 烧杯+稀盐酸质量 | 139 g | 129 g | 129 g |
| 加入黄铜样品质量 | 20 g | 24 g | 20 g |
| 充分反应后,烧杯+剩余物质质量 | 158.8 g | 152.8 g | 148.8 g |
请回答下列问题:
(1)____同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是______。
(2)计算黄铜样品中锌的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
分析下列图像,按要求回答问题:
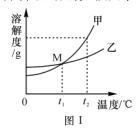
(1)图Ⅰ中M点表示的意义是________________________;甲、乙两种物质的溶解度受温度影响较大的是_____。
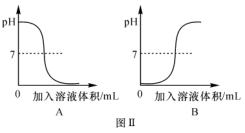
(2)图Ⅱ是中和反应过程中溶液pH变化的图像,其中能表示向氢氧化钠溶液 中滴加稀盐酸的是____(填“A”或“B”),若在氢氧化钠溶液中预先滴加酚酞试液,则在滴加稀盐酸的过程中溶液颜色的变化为____________________。
中滴加稀盐酸的是____(填“A”或“B”),若在氢氧化钠溶液中预先滴加酚酞试液,则在滴加稀盐酸的过程中溶液颜色的变化为____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
化学与健康——从化学的视角看食品添加剂。从化学的视角看食品添加剂,主要是从其元素组成与结构、物理化学性能及在人体内的变化等方面来研究。结合表中信息回答下列问题:
| 物质的组成与性能 | 用于食品添加剂 | |||
| 物质名称 | 物质组成 | 主要化学性质及在体内变化 | 类别或作 | 法律规定 |
| 碳酸氢钠严格 | NaHCO3 | 无毒、弱碱性,易与胃酸反应,加热分解成碳酸钠、水和二氧化碳 | 膨松剂 | 可用 |
| 铁(还原性铁粉) | Fe | 比较活泼的金属,能与胃酸反应 | 抗氧化剂 | 依据国家标准可用 |
| 食盐 | NaCl | 易溶、中性,与硝酸银溶液反应生成白色沉淀 | 调味剂 | 可用 |
| 甲醛 | CH2O | 防腐 | 国家严禁使用 | |
| 亚硝酸钠 | NaNO2 | 易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 | 发色剂、防腐剂 | 依据国家标准 |
(1)国家严格禁止甲醛作为食品添加剂的原因是_______________________________。
(2)还原性铁粉用于食品添加剂,除能够防止食品因氧化而变质外,还是一种营养强化剂,这是因为______。
(3)碳酸氢钠是面食类食品经常使用的添加剂,如蒸馒头时人们常常加适量的碳酸氢钠,其作用是_______,写出发生反应的化学方程式_________________。
(4)亚硝酸钠(NaNO2)外观酷似食盐,有咸味,常被误作食盐食用而导致中毒事件发生。有一包外观酷似食盐的固体,结合表中信息,如何鉴别它是亚硝酸钠还是氯化钠?_____________________________________________________。
(包括选取的试剂、方法、实验现象和结论,只写出一种方法即可)。
(5)从改善食品的色香味、延长食品的保质期等方面看,食品添加剂确实提高了现代食品的品质,但副作用也是显而易见的。我们需要食品添加剂吗?你的观点是____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列各组物质的溶液不用其他试剂就可鉴别的是( )
A.HCl CuSO4 KNO3 Na2SO4 B.FeCl3 HCl NaCl NaOH
C.CaCl2 K2CO3 HCl (NH4)2CO3 D.NaNO3 Na2SO4 HCl H2SO4
查看答案和解析>>
科目:初中化学 来源: 题型:
碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)为常见的两种化合物,其中碳酸钠最为重要,在工业上有广泛的应用。在生活中,碳酸氢钠是常用的发酵剂的主要成分。
Ⅰ.(1)碳酸钠和碳酸氢钠中阴离子对应的酸都是 (填化学式)
(2)碳酸氢钠在医疗上用作治疗胃酸过多,反应的化学方程式为 。
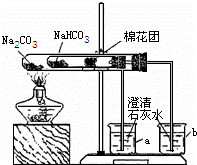 Ⅱ.某天然碱中可能含有碳酸钠和碳酸氢钠,小明同学设计了如下实验探究其组成。请分析其过程完成填空。
Ⅱ.某天然碱中可能含有碳酸钠和碳酸氢钠,小明同学设计了如下实验探究其组成。请分析其过程完成填空。
在老师的指导下采用了右图所示装置用小苏打和纯碱做了对比实验。实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊。试回答:① 结论: (填“碳酸钠”或“碳酸氢钠”)受热分解出水和CO2等物质 ;②写出b烧杯中发生反应的化学方程式 。
同学们还查阅到如下资料:
(1)2NaHCO3+ Ca(OH)2= Na2CO3 +CaCO3↓+H2O
(2)Ca(HCO3)2 +Na2CO3= CaCO3↓+2NaHCO3
(3)CaCl2 稀溶液与 NaHCO3稀溶液混合无沉淀、与Na2CO3稀溶液混合有沉淀
【假设猜想】
假设一:天然碱成分为碳酸氢钠;
假设二:天然碱成分为碳酸钠;
假设三:天然碱成分为 。
【实验方案】
方案一:取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成 立都能进行判断。请评价这种方案是否合理 (填“是”或“否”),理由是 。
立都能进行判断。请评价这种方案是否合理 (填“是”或“否”),理由是 。
方案二:
可选药品:NaOH溶液 稀盐酸 Ca(OH )2溶液 CaCl2溶液
)2溶液 CaCl2溶液
| 实验操作 | 实验现象 | 实验结论 |
| 操作一:取天然碱样品少量溶于足量水后,加入过量的 (如果操作一有沉淀,则进行操作二) | 无沉淀出现 | 假设一成立 |
| 操作二:待操作一中反应充分后过滤,并在滤液中加入过量的 ,观察。 |
| 假设二成立 |
|
| 假设三成立 |
Ⅲ.为测定天然碱中的成分,小组的同学设计了如下实验,其主要实验步骤如下:
(1)按图组装仪器,将52.5g试样放入锥形瓶中,打开活塞B,从导管A处缓缓鼓入一定量的空气;
(2)准确称量干燥管的质量后再次连接好装置;
(3)关闭活塞B,打开分液漏斗的活塞和上面的塞子,加入足量某酸溶液;
(4)待锥形瓶中不再产生气泡时,打开活塞B,再次从导管A处缓缓鼓入一定量的空气,直至干燥管内物质质量不变;
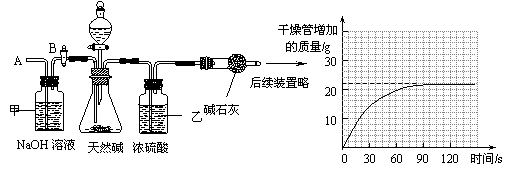
(5)再次称量干燥管的质量;并绘制干燥管增加的质量与时间的关系图(见下图);
 |
| |
讨论:
①步骤(1)加入样品前还应 ,所加的酸溶液最好是 。
②装置甲的作用是 ;装置乙的作用是 。第(4)步再次从导管A处缓缓鼓入一定量的空气的作用是 。
③请利用有关数据计算试样中碳酸氢钠的质量分数。(写出计算过程)(2分)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com