
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| 1.将NaOH溶液加热煮沸 | 溶液变红,过一会儿红色消失 | 甲同学猜想 | |
| 2.向冷却后的溶液中滴入酚酞,并滴一些植物油在其上方 |
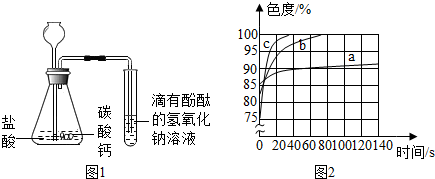
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| 1.将NaOH溶液加热煮沸 | 除去氢氧化钠溶液中溶解的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想 不正确(填“正确”或“不正确”) |
| 2.向冷却后的溶液中滴入酚酞,并滴一些植物油在其上方 | 隔绝氧气 |
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| 1.将NaOH溶液加热煮沸 | 除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想不正确 |
| 2.向冷却后的溶液中滴入酚酞,并滴一些植物油在其上方 | 隔绝氧气 |


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:初中化学 来源: 题型:
| A、不锈钢 | B、玻璃 |
| C、铝合金 | D、铜线 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
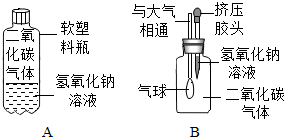 在化学课堂上,我和同学们一起进行对碱的化学性质的探究:将二氧化碳分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.澄清石灰水变浑浊的原理:
在化学课堂上,我和同学们一起进行对碱的化学性质的探究:将二氧化碳分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.澄清石灰水变浑浊的原理:| 实验步骤 | 实验现象 | 实验结论 |
| 向B实验后的溶液中加入 | | 猜想①成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com