
分析 【假设与猜想】根据质量守恒定律进行猜想;
根据猜想进行试验设计;
【证据与结论】根据实验设计和物种的性质分析解答;
【分析与交流】(1)CO与CuO反应生成了CO2;(2)若将乙炔燃烧的产物依次通入足量的浓硫酸和足量的澄清石灰水,浓硫酸和澄清石灰水的顺序倒过来并不能起到干燥气体的作用,再将剩余气体通过炽热的氧化铜,此时氧化铜不变红,不能说明没有还原性气体,因为查阅资料可知当还原性气体中混有水蒸汽时,则难以还原氧化铜;据此解答.
解答 解:【假设与猜想】质量守恒定律可知,乙炔燃烧的产物中除水外主要还有二氧化碳,如果燃烧不充分,还会有一氧化碳;
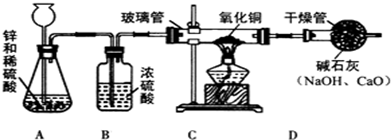
将乙炔燃烧的产物依次通入足量的A试剂和足量的浓硫酸,将剩余气体通过炽热的氧化铜,足量的浓硫酸,可以除去水蒸气,将剩余气体通过炽热的氧化铜,若氧化铜变红,说明有CO.所以A试剂可以验证二氧化碳,二氧化碳能够使澄清的石灰水变浑浊,A试剂是澄清的石灰水;
【证据与结论】
实验(1):二氧化碳能够使澄清的石灰水变浑浊,观察到A试剂的瓶中澄清的石灰水变浑浊,说明一定有二氧化碳,
(2)足量的浓硫酸,可以除去水蒸气,将剩余气体通过炽热的氧化铜,若氧化铜变红,说明有CO.
【分析与交流】(1)若将乙炔燃烧的产物先通入足量的浓硫酸,再依次通过灼热的氧化铜;CO与CuO反应生成了CO2,再通入足量A试剂,无法证明二氧化碳是原有的二氧化碳,还是CO与CuO反应生成得CO2,无法证明二氧化碳是否存在;
(2)若将乙炔燃烧的产物依次通入足量的浓硫酸和足量的澄清石灰水,除去了二氧化碳,但由于把浓硫酸放在前面,后面再通入澄清石灰水,浓硫酸不能起到干燥气体的作用,再将剩余气体通过炽热的氧化铜,此时氧化铜不变红,不能说明没有一氧化碳,因为查阅资料可知当还原性气体中混有水蒸汽时,则难以还原氧化铜.
故答案为:
【假设与猜想】①二氧化碳
澄清石灰水
【证据与结论】实验(1)澄清的石灰水变浑浊;实验(2)黑色粉末变红色;
分析与交流:(1)不能;原因是CO与CuO反应生成了CO2
(2)不能.
点评 本题属于信息题的考查,熟悉质量守恒定律、一氧化碳、二氧化碳的性质是解题的关键.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
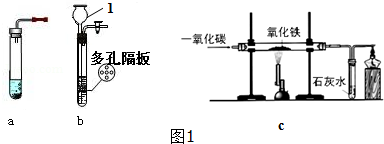 如图1所示装置制取氢气,试回答下列问题:
如图1所示装置制取氢气,试回答下列问题:
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 都能确定 | B. | 都不能确定 | ||
| C. | 除④和⑥外都能确定 | D. | 只有①和⑤能确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应前 | 反应后 | |
| 烧杯及其中物质的质量 | 136.0g | 135.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 属于氧化物 | |
| B. | 碳、氢、氧三种元素质量比是22:34:3 | |
| C. | 氢元素的质量分数最大 | |
| D. | 由三种非金属元素组成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com