
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源:2013届江苏省无锡市宜兴实验学校九年级5月中考适应性考试化学试卷(带解析) 题型:探究题
我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a. b. c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验: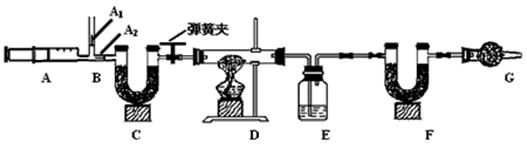
资料:
1. 许多物质从水溶液里析出晶体时,晶体里常含有一定数目的水分子,这样的水分子叫做结晶水。含有结晶水的物质叫做结晶水合物。
天然碱样品(aNa2CO3·bNaHCO3·cH2O)是一种结晶水合物,受热时结晶水易失去;
2. 2NaHCO3  Na2CO3↑+CO2 ↑+H2O ;
Na2CO3↑+CO2 ↑+H2O ;
3. 碳酸钠比较稳定,加热时不分解。
4.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
(一)实验步骤:①组装好装置,检查气密性 ②反复推拉注射器 ③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量。
(二)问题探究:
(1)E中的药品为 ;C、F、G中装有碱石灰(CaO与NaOH的固体混合物)
G的作用是 。
(2)若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数 (填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是 。
(3)请你根据下表数据计算:该天然碱样品16.6g中碳酸氢钠的质量(写出具体计算过程)。
| 组别 | 反应前 | 反应后 |
| 甲 | E的质量为100.0克 | E的质量为102.25克 |
| 乙 | F的质量为50.0克 | F的质量为51.1克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

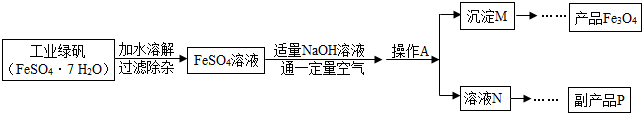
 Fe3O4+4H2O,控制“一定量空气”的目的是______,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为______.
Fe3O4+4H2O,控制“一定量空气”的目的是______,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为______.查看答案和解析>>
科目:初中化学 来源:2011年江苏省苏州市高新区中考化学模拟试卷(解析版) 题型:填空题

 Fe3O4+4H2O,控制“一定量空气”的目的是,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为.
Fe3O4+4H2O,控制“一定量空气”的目的是,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com