
【题目】每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁生锈有弊也有利。一化学兴趣小组对某月饼包装盒中的“脱氧剂”很好奇,他们观察到“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末。
(资料获悉)①铁系“脱氧剂”的作用原理是利用铁能被氧气氧化,从而达到除氧保鲜的目的。铁被氧气氧化最终产物为红棕色的Fe2O3(其他产物忽略不计)。
②Fe2O3+3H2SO4═Fe2(SO4)3+3H2O; Fe+Fe2(SO4)3═3FeSO4。
③“碱石灰的干燥管”可以用来干燥氧气、氢气等气体。
④铁、活性炭、Fe2O3固体不溶于水,Fe2(SO4)3、NaCl、FeSO4固体能溶于水。
(探究目的)小组同学欲探究该“脱氧剂”是否已经失效,并测定10.00g样品各成分的质量,设计了以下探究实验。
(实验探究)(假设所有操作没有损失)
步骤1:小刚用磁铁接近样品,发现磁铁吸引了部分黑色固体。
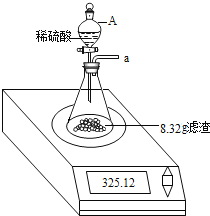
步骤2:称取10.00g样品于一烧杯中,加足量水充分搅拌溶解后,过滤,将滤渣洗涤、干燥、称得其质量为8.32g。
步骤3:按如图装置,将得到的8.32g固体与足量稀硫酸反应,用电子秤称得反应前后总质量差为0.11g。
步骤4:将锥形瓶中反应后的液体过滤,并将滤渣洗涤、干燥后,称得其质量为1.20g。
步骤5:分析测算步骤4中所得滤液得知:滤液中溶质是硫酸和硫酸亚铁,且最后通过结晶分离出16.72g硫酸亚铁。
(交流讨论)
(1)由步骤1得出的结论是_____。
(2)步骤2目的是除去并测得_____的质量,得知该物质的质量为_____g。
(3)步骤4中滤渣的主要成分是_____,若没有经过洗涤,则称得的质量_____1.20g(填“>”或“=”或“<”)
(4)小刚认为0.11g差值即为H2的质量,并由此计算出样品中单质铁的质量为3.08g。小华提出在装置的a导管处应该再连接一个盛有碱石灰的干燥管,他这样做的理由是_____。
(5)小华还认真分析题中所给资料,他认为用产生H2的质量计算样品中所含铁的质量不合理,其理由是:_____。
(学生实验)小华将步骤3的装置进行了改进,重新称取10.00g样品进行实验,并准确测得固体与足量稀硫酸反应前后总质量差为0.1g。
(6)请根据以上数据,计算10g该样品中各成分的铁和氧化铁的质量。(只写出结果)铁:_____g,氧化铁:_____g。
【答案】“脱氧剂”没有完全失效 氯化钠 1.68 活性炭 > 防止水蒸气随氢气“跑”到装置外面 样品中的铁,除了与稀硫酸反应生成氢气外,还有一部分铁与硫酸铁溶液反应 2.8g 4.32g
【解析】
交流讨论:
(1)铁能被磁铁吸引,由步骤1得出的结论是“脱氧剂”没有完全失效。
(2)“脱氧剂”的成分为铁粉、活性炭和氯化钠,步骤2中加水溶解,过滤、洗涤,目的是除去并测得氯化钠的质量,得知该物质的质量为10-8.32g=1.68g。
(3)“脱氧剂”的成分中活性炭不溶于水也不与稀硫酸反应,步骤4中滤渣的主要成分是活性炭,若没有经过洗涤,滤渣上附有溶质,则称得的质量>1.20g。
(4)反应在溶液中进行,在装置的a导管处应该再连接一个盛有碱石灰的干燥管,这样做的理由是防止水蒸气随氢气“跑”到装置外面。
(5)铁与硫酸铁也能发生反应,用产生氢气的质量计算样品中所含铁的质量不合理,理由是:样品中的铁,除了与稀硫酸反应生成氢气外,还有一部分铁与硫酸铁溶液反应。
学生实验:
(6)设生成0.1g氢气需要铁的质量为x,则
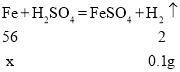
![]()
解得x=2.8g;
故氧化铁的质量为10g-1.68g-1.2g-2.8g=4.32g。


 全能练考卷系列答案
全能练考卷系列答案科目:初中化学 来源: 题型:
【题目】化学兴趣小组的甲、乙、丙三位同学发现实验台上有一瓶标签残缺的试剂(如图),他们对此进行了如下探究。
![]()
(提出问题)这是一瓶什么溶液?
(猜想与假设)甲同学的猜想是Na2SO3溶液;乙同学的猜想是Na2SO4溶液,你的猜想是____(写化学式,只写一种)。
(查阅资料)
(1)白色沉淀BaSO3不溶于水,但能溶于稀盐酸。
(2)硝酸具有强氧化性,能将BaSO3被氧化成BaSO4。
(3)Na2SO3与稀盐酸反应产生无色气体SO2,SO2能使澄清石灰水变浑浊,也能使品红溶液褪色。
(进行实验)
I.甲同学取适量的该溶液于试管中,滴加稀盐酸产生无色气体,甲同学认为自己的猜想成立,而乙同学认为甲的结论不合理,原因是______________________________________________。
II.乙同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量稀硝酸,现象为___________,乙同学认为自己的猜想成立。
III.激发丙同学对乙同学的猜想又提出了质疑,丙认为加BaCl2和稀硝酸,Na2SO3也能产生沉淀,为了验证自己的观点,做了如下实验:
步骤 | 操作 | 实验现象 | 实验结论 |
步骤1 | 取少量该溶液于试管中滴加足量的BaCl2溶液 | ______。 | 无 |
步骤2 | 向步骤1的试管中滴加足量的稀盐酸溶液 | _____。 | 此溶液不是Na2SO4溶液。 |
步骤3 | 将步骤2中产生的气体通入品红溶液 | 品红溶液褪色。 | ____。 |
写出丙同学实验过程中的化学方程式:____________________________,_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的基本工具,请用化学符合或化学式填空:
(1)2个铁原子________;
(2)氦气_________;
(3)5个一氧化碳分子___________;
(4)2个铵根离子________;
(5)最清洁的气体燃料__________;
(6)3个亚铁离子______________
(7)标出五氧化二磷中磷的化合价_________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】被称为“第四类新材料”的玉米塑料学名叫“聚乳酸”,它是生物环保材料,可由乳酸(C3H603)合成而得,下列说法正确的是
A.乳酸中C、H、0三种元素的量比为1:2:1
B.乳酸的相对分子质量为90g
C.90g乳酸完全燃烧时生成的二氧化碳质量132g
D.乳酸是有机高分子化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸钾和氯化钾的溶解度曲线如图所示:
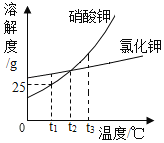
(1)t1℃时,硝酸钾的溶解度为_____。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液的质量为_____。
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是_____。
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t2℃过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是_____。
A 都是饱和溶液
B 溶液质量a<b
C 溶质质量a=b
D 溶剂质量a<b
E.溶质的质量分数a=b
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学教师在通风橱里表演了小魔术“无中生有”:如图1所示,相同条件下,A、B两个体积相同的集气瓶中分别充满无色的硫化氢(H2S)气体和二氧化硫气体.抽开毛玻璃片,瓶口对紧,颠倒几次,使两种气体充分混合。一会儿,观察到两瓶内壁附着淡黄色固体颗粒。请回答下列问题:
(1)若用“●”表示氢原子,用“○”表示氧原子,用“![]() ”表示硫原子,上述反应过程可用如图2表示:
”表示硫原子,上述反应过程可用如图2表示:
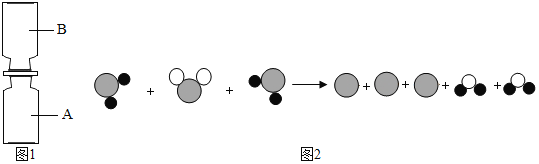
该反应的化学方程式为_____;
(2)若这两个瓶子是质地较软的塑料瓶,我们将会观察到塑料瓶变瘪了,原因是_____。
(3)已知:相同条件下,相等体积的气体所含的分子数目相等。反应完毕,瓶中剩余的气体为_____,处理该气体的方法(用化学方程式表示)是_____。;
(4)某同学对H2S气体很感兴趣,通过查资料得知:H2S气体有臭鸡蛋气味,水溶液是一种酸。他将H2S气体通入硫酸铜溶液中,发现有黑色沉淀生成,同时溶液的酸性增强。试写出有关反应方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纳米小人的英语是Nanoputian,这是James M Tour 教授发明的一个合成词。Nanoputian 是一些拟人的有机分子,它们都是通过分子电子学研究中常用的有机结构单元组合起来的, 但又同时充满了创意。如图为某纳米小人(C39H42O2)的结构简式。下列关于C39H42O2分子的说法正确的是( )
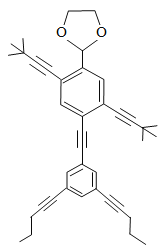
A.1 个分子中含有 1 个氧分子
B.由碳、氢、氧三种元素组成
C.1 个分子中含有 83 个原子
D.碳元素与氢元素的质量比为 13:14
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2016年里约奥运会火炬由再生铝和树脂材料制造而成,火炬的整体外观轮廓体现了“运动、创新与巴西风格”。
(1)工业上常用通电分解氧化铝(Al2O3)制备单质铝,同时生成了氧气,则该反应的化学方程式为________,该反应的基本类型为______。
(2)火炬的外壳用铝合金制作有利于火炬手收藏火炬。其原因是铝在空气中易氧化而形成一层___________,保护铝制品不被继续腐蚀。请你还说出利用铝合金材料的其他优点(至少一点)___________________。
(3)采集奥林匹克圣火,在奥林匹克的赫拉神庙前利用凹面镜集中阳光来引燃火种。阳光为火种的燃烧提供了_________。火炬燃烧时,_______能转化为热能和光能。
(4)火炬燃烧系统内装环保型燃料丙烷(C3H8 ),丙烷属于_____(选“无机”或“有机”)化合物。当火炬点燃后,所发生反应的化学方程式为__________,所用燃料符合“绿色奥运”的要求,原因是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锌锰电池(俗称干电池)在生活中的用量很大.锌锰电池的构造如图所示.请回答下列问题:
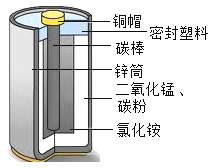
(1)锌锰电池所使用的下列材料中,属于金属材料是___,属于合成材料的是___(填序号)。
A铜帽 B碳棒 C锌筒 D密封塑料
(2)废旧电池铜帽会生成一些绿色的铜锈,其主要成分为Cu2(OH)2CO3,化学式表明铜生锈除了水和氧气外,还必须有___参与。
(3)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,该反应中锰元素的化合价由+4变为______。
(4)利用废旧电池铜帽(含铜、锌)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去):
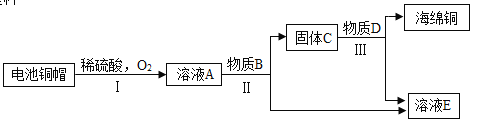
已知:2Cu+2H2SO4+O2![]() 2CuSO4+2H2O
2CuSO4+2H2O
①过程Ⅲ中的分离操作名称为______;
②过程Ⅱ发生的化学反应方程式为 ______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com