
| A. | 青铜的硬度比铜大 | B. | 青铜属于金属材料 | ||
| C. | 青铜属于纯净物 | D. | 青铜耐腐蚀,易铸造成形 |
科目:初中化学 来源: 题型:实验探究题
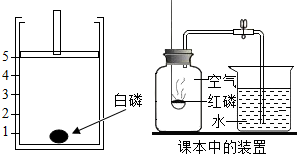 为测定空气中氧气所占的体积分数,某同学设计了如图实验,在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,可以观察到的现象为白磷燃烧产生大量白烟;冷却至原来温度时,慢慢松开手,活塞最终将回到刻度4处,但是实验结果往往偏低,其原因可能是白磷的量不足或没有等到装置冷却就读数(只写一种),试回答白磷燃烧的原因压缩活塞使装置内的温度升高,达到白磷的着火点,且装置里有空气.该装置与课本中的实验装置相比,优点是环保无污染.
为测定空气中氧气所占的体积分数,某同学设计了如图实验,在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,可以观察到的现象为白磷燃烧产生大量白烟;冷却至原来温度时,慢慢松开手,活塞最终将回到刻度4处,但是实验结果往往偏低,其原因可能是白磷的量不足或没有等到装置冷却就读数(只写一种),试回答白磷燃烧的原因压缩活塞使装置内的温度升高,达到白磷的着火点,且装置里有空气.该装置与课本中的实验装置相比,优点是环保无污染.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2CO3═H2O+CO2↑ | B. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | 2HCl+CuO═CuCl2+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
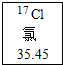 元素周期表是学习化学的重要工具,如图所示是周期表的一格.
元素周期表是学习化学的重要工具,如图所示是周期表的一格.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com