考点:氢气的制取和检验,实验探究物质的组成成分以及含量,气体的净化(除杂),实验室制取氧气的反应原理,书写化学方程式、文字表达式、电离方程式,氢气的化学性质与燃烧实验,氢气、一氧化碳、甲烷等可燃气体的验纯
专题:常见气体的实验室制法、检验、干燥与净化,科学探究
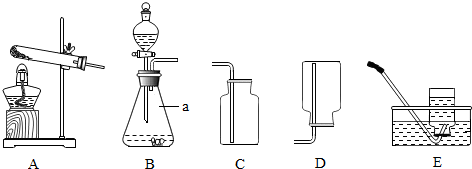
分析:根据图为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器.可知:
(1)某同学以锌粒和稀盐酸为原料在实验室制备、收集纯净干燥的氢气,则除掉氯化氢气体、干燥;因为氢气的可燃性,在点燃氢气之前一定要检验氢气的纯度.根据反应物、生成物,正确书写化学方程式.
(2)若以H
2O
2溶液和MnO
2在实验室中制备干燥的氧气,并用来测定B装置中盛有的Cu和C混合物中Cu的含量,取ag混合物样品放入装置B的硬质玻璃管中,所选仪器连接顺序为:A-D-B-C,根据图中仪器,可知:仪器D的作用和仪器B中的现象.
根据“若通入足量氧气充分反应后,测得B装置中硬质玻璃管内固体的质量在反应前后无变化”,则碳和氧气反应生成二氧化碳,铜和氧气反应生成氧化铜,充分反应后B装置中大试管内剩余的固体为氧化铜,a氧化铜中铜元素的质量为a×
=6.4g,所以原混合物中铜元素的质量分数为
.
考虑氧化铜与稀硫酸的反应.
解答:解:
根据图为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器.可知:
(1)①某同学以锌粒和稀盐酸为原料在实验室制备、收集纯净干燥的氢气,则除掉氯化氢气体、干燥,所选装置的连接顺序为 A E D F;
②因为氢气的可燃性,在点燃氢气之前一定要检验氢气的纯度.
③该同学制备氢气发生反应的化学方程式 Zn+2HCl═ZnCl
2+H
2↑.
(2)若以H
2O
2溶液和MnO
2在实验室中制备干燥的氧气,并用来测定B装置中盛有的Cu和C混合物中Cu的含量,取ag混合物样品放入装置B的硬质玻璃管中,所选仪器连接顺序为:A-D-B-C,根据图中仪器,可知:
①仪器D的作用是干燥氧气.
②仪器B中的现象是红色的固体变黑.
③根据“若通入足量氧气充分反应后,测得B装置中硬质玻璃管内固体的质量在反应前后无变化”,则碳和氧气反应生成二氧化碳,铜和氧气反应生成氧化铜,充分反应后B装置中大试管内剩余的固体为氧化铜,a氧化铜中铜元素的质量为a×
,所以原混合物中铜元素的质量为
.
④欲用化学方法证明硬质玻璃管内的固体在通入氧气后完全发生了反应,则可设计实验方案,并简述操作步骤、现象和结论 取玻璃管内固体加入稀硫酸,若固体全都溶解得到蓝色溶液,则固体在通入氧气后完全发生了反应故答案为:
(1)①A E D F;②检验氢气的纯度;③Zn+2HCl═ZnCl
2+H
2↑
(2)①干燥氧气; ②红色的固体变黑; ③
;
④取玻璃管内固体加入稀硫酸,若固体全都溶解得到蓝色溶液,则固体在通入氧气后完全发生了反应.
点评:熟记实验室制取氢气的反应原理、注意事项以及物质的检验和除杂的知识等,并能灵活应用质量守恒定律和相关知识进行解题,要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.




 如图是某品牌胃药的部分标识.胃药中所含的物质能中和胃里过多的胃酸(主要成分是盐酸).某患者按标识上的服用方法服药三天后病情好转.
如图是某品牌胃药的部分标识.胃药中所含的物质能中和胃里过多的胃酸(主要成分是盐酸).某患者按标识上的服用方法服药三天后病情好转.