
【题目】稀土元素铕(Eu)是激光及原子能应用的重要材料.已知氯化铕的化学式为EuCl3,则氧化铕的化学式为( )
A.Eu2O3 B.EuO C.Eu3O2 D.EuO3
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下:

①反应A的基本反应类型是 (14) ,反应B的化学方程式为 (15) 。
②流程中的H2可以做燃料,在空气中充分燃烧的化学方程式是 (16) ;工业上常常利用H2冶炼钨、钼等金属,是利用了H2的 (17) (填“氧化性”或“还原性”)。
③操作a的名称是 (18) ,进行此操作时玻璃棒的作用是 (19) 。
④写出NH4Cl的一种用途 (20) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析下表数据,与深冷法相比,变压吸附法的优点是 。
项目 | 变压吸附法 | 深冷法 |
最大产量(m3/h) | 3200 | 20000 |
产品气含氧量(%) | 93~95 | 99.5~99.8 |
工作表压强(kPa) | -70~40 | 460~750 |
温度(℃) | 0~40 | -109~-190 |
产每立方米氧气耗电量(kW·h) | 0.40 | 0.50~0.65 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取氯酸钾和二氧化锰的混合物26 g,加热至混合物固体质量不再减少为止,冷去然后称得剩余固体质量为16.4 g,将剩余固体加入一定量的水中,充分搅拌后过滤,滤液是10 %的氯化钾溶液(假设溶液无损失)。计算:
(1)生成氧气的质量。
(2)参加反应的氯酸钾的物质的量。(根据化学方程式列式计算)。
(3)氯化钾溶液的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锌锰电池(俗称干电池)其构造如右图所示。
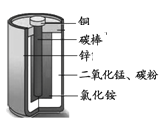
①根据右图判断,属于金属材料的是____(15)___。
②易溶于水的氯化铵固体中混有难溶物二氧化锰,提纯氯化铵固体的实验步骤是:溶解、__(16)_____、结晶。
③利用废旧电池样品(含Cu、Zn)回收铜(Cu),并得到硫酸锌溶液,主要流程如下图所示:
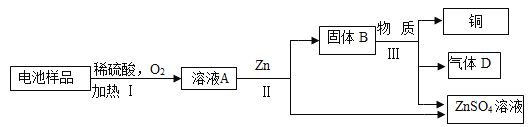
![]() 已知:2Cu+O2+2H2SO4
已知:2Cu+O2+2H2SO4 ![]() 2CuSO4+2H2O过程中 I中稀硫酸过量的目的是 (17) ;过程II中发生金属间置换反应的化学方程式为 (18) ;气体D是 (19) 。
2CuSO4+2H2O过程中 I中稀硫酸过量的目的是 (17) ;过程II中发生金属间置换反应的化学方程式为 (18) ;气体D是 (19) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验基本操作在化学学习中具有重要作用.现有a试管、b漏斗、c酒精灯、d集气瓶、e药匙、f胶头滴管等仪器,请为下列实验操作各选一种(用序号填空).
(1)可以直接在酒精灯上加热的仪器是 ;
(2)吸取或滴加少量液体使用 ;
(3)取用粉末状固体药品应用 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】各种微粒构成了宏观世界,下列说法正确的是
A.原子中一定含有质子和中子
B.相对原子质量越大,原子的实际质量越小
C.如果规定以质子数和中子数都为8的氧原子质量的1/8为标准,则碳-12原子的相对原子质量为6
D.氦-3原子的核内有3个质子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组的同学围绕着LNG船舶使用的金属材料进行了研究。
【阅读与思考】(1)在焊接不锈钢管道时,通常要使用氩气作保护气,这是因为氩气的化学性质 。
(2)金属在海水中易生锈腐蚀。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌另外一种金属。利用该金属与铁的活动性的不同,保护铁不易被腐蚀。

【研究课题1】一般情况下,两种活动性不同的金属在潮湿的环境中接触时,哪种金属先被腐蚀呢?
【实验设计1】将打磨后的金属片进行如图1所示的实验,放置一段时间后将观察到的现象及分析填入下表:
现象 | 分析 |
甲中:铝片表面出现灰白色物质,铁片表面几乎没有明显现象。 | 铝与铁在潮湿的环境中接触, 首先被腐蚀。 |
乙中:铁片表面出现 ,铜片表面几乎没有明显现象。 | 铁与铜在潮湿的环境中接触,铁首先被腐蚀。 |
【得出结论】一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较 填“强”或“弱”)的金属首先被腐蚀。
【知识应用】造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是 (填编号)。
A.银块 B.铜块 C.锡块 D.锌块
(3)LNG船还使用了大量的锌铜合金。
【研究课题2】测定锌铜合金中铜的质量分数
【实验设计2】进行如图2所示的实验。
(1)图中量气管和水准管可用来测量气体体积,为准确测量氢气的体积,在读取量气管中液面读数的过程中,应注意 (填编号)。
A.读数时视线与凹液面最低处相平
B.读数前应上下移动水准管,待两管液面相平再读数
C.保持水准管静止,待水准管中液面不再上升时再读数
(2)实验前,将已经打磨过的块状锌铜合金加工成碎屑,其目的是: 。
(3)实验操作步骤:检查气密性,将药品和水装入各仪器中,连接好装置后,再次检查装置的气密性,记录量气管的液面位置为5mL,由A向B滴加足量试剂,待B中不再有气体产生并恢复至室温后,记录量气管的液面位置为85mL;将B中剩余固体过滤,洗涤,干燥,用电子天平称其质量为0.416g。
【数据处理】该实验条件下,氢气的密度是0.09gL﹣1.根据上述的数据计算锌铜合金中铜的质量分数。
(请在答题卡上写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com