
分析 (1)根据有机物和无机物的区别来分析;
(2)根据物质的分子结构来分析;
(3)根据化合物中元素的质量比来分析;
(4)碱性溶液能与酸性氧化物反应生成盐和水.
解答 解:(1)苯并芘是一种含碳元素的化合物,属于有机物;亚硝酸胺中不含碳元素,不属于有机物、铅属于金属单质、一氧化碳是一种含碳元素的化合物,但是其性质与无机物相似,不属于有机物;故填:C20H12;
(2)一个亚硝酸胺(化学式为NH4NO2)是由2个氮原子、4个氢原子和2个氧原子,故氮、氢、氧元素的原子个数比2:4:2=1:2:1,故填:1:2:1;
(3)亚硝酸胺中,氮、氢、氧三种元素的质量比为:(14×2):(1×4):(16×2)=7:1:8,可见其中氧元素的质量分数最大,故填:氧;
(4)二氧化氮能与水反应生成硝酸和亚硝酸,硝酸和氢氧化钙反应生成硝酸钙和水,亚硝酸和氢氧化钙反应生成亚硝酸钙和水,完全反应后溶液中的溶质是硝酸钙和亚硝酸钙.
故填:Ca(NO3)2、Ca(NO2)2.
点评 本题主要考查了物质的分类方法和有关化学变化的问题,完成此题,可以依据题干提供的信息结合物质的性质进行.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
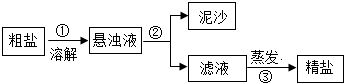 食盐、纯碱、小苏打、碳酸钙、硫酸铜等盐在生活中有广泛用途.
食盐、纯碱、小苏打、碳酸钙、硫酸铜等盐在生活中有广泛用途.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
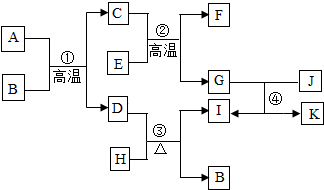
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
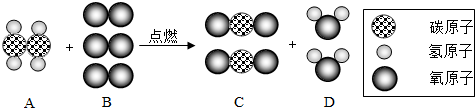
| A. | 该反应属于置换反应 | |
| B. | 生成物中物质C与物质D都是氧化物 | |
| C. | 参加反应的A、B两物质的质量比为1:3 | |
| D. | 反应前后氧元素的化合价没有改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 钙是维持人体正常功能所必需的元素,有时需要服用补钙剂来满足人体的需求.如图所示的是某钙片的说明书.求:
钙是维持人体正常功能所必需的元素,有时需要服用补钙剂来满足人体的需求.如图所示的是某钙片的说明书.求:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
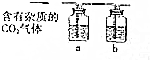 化学复习课上,某实验小组同学利用盐酸与大理石反应制取二氧化碳时,发现产生的气体经反复实验也不能使澄清石灰水变浑浊.
化学复习课上,某实验小组同学利用盐酸与大理石反应制取二氧化碳时,发现产生的气体经反复实验也不能使澄清石灰水变浑浊.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
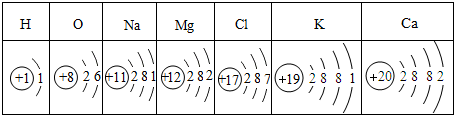
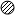 ”和“
”和“ ”分别表示两种不同的原子,其中表示化合物的是D,表示混合物是BC,表示单质的是A.
”分别表示两种不同的原子,其中表示化合物的是D,表示混合物是BC,表示单质的是A.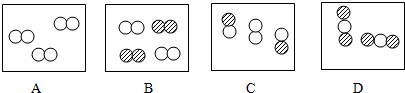
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com