
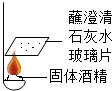
 在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:
在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:| 方案 | 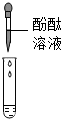 | 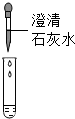 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 溶液中有氢氧化钠 | 溶液中由碳酸钠 |
分析 【实验探究】
二氧化碳能使澄清石灰水变浑浊;
氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
显碱性的溶液能使酚酞试液变红色;
碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
【反思交流】
碳酸钠能和氯化钡反应生成白色沉淀碳酸钡和氯化钠;
【拓展应用】
氢氧化钡和碳酸钠反应生成白色沉淀碳酸钡和氢氧化钠,氢氧化钙和碳酸钠反应生成白色沉淀碳酸钙和氢氧化钠.
解答 解:【实验探究】
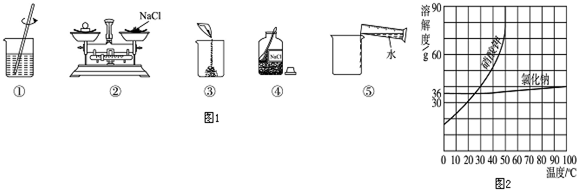
(1)按如图实验,发现澄清石灰水变浑浊,说明酒精燃烧生成了二氧化碳,进一步说明固体酒精中含碳元素.
故填:含.
(2)取少量“固体酒精”放在烧杯中,加足量的水充分搅拌后,静置,发现烧杯底部有白色沉淀,白色沉淀是氢氧化钠和二氧化碳反应生成的碳酸钠和氯化钙反应生成的碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
分析实验可知,氢氧化钠已经变质,和二氧化碳反应生成了碳酸能和水.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;已经.
(3)①甲组烧杯中的上层溶液放在两支试管中,探究过程如下表所示:
| 方案 | 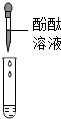 | 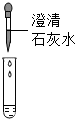 |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 溶液中有氢氧化钠 | 溶液中有碳酸钠 |
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | Hg由原子构成,H2由分子构成 | |
| B. | 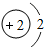 和 和 最外层都有2个电子,化学性质相似 最外层都有2个电子,化学性质相似 | |
| C. | X原子的核内质子数为n,该原子核外电子数也为n | |
| D. | 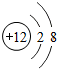 、 、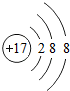 ,分别表示Mg2+和Cl- ,分别表示Mg2+和Cl- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 石蕊试液 | 氯化钡溶液 | |
| 甲车间 | 变蓝色 | 产生白色沉淀 |
| 乙车间 | 变红色 | 无明显现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
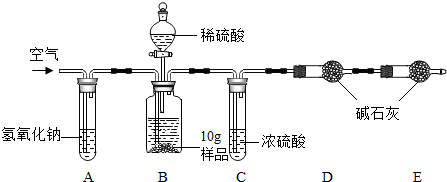
| 实验步骤 | 实验现象 | 解释或结论 |
| 取适量烧碱样品置于试管中,加水溶解,向所得的溶液中逐滴加入过量的稀硝酸. | 开始时无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体 | 样品中含有的杂质是碳酸钠. |
| 向上述所得的溶液中滴加几滴AgNO3溶液 | 产生白色沉淀 | 样品中还含有的杂质是氯化钠. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
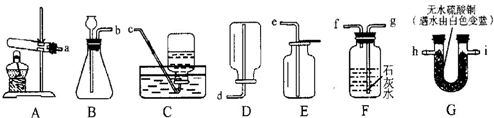
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 40% | B. | 45% | C. | 30% | D. | 70% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com