
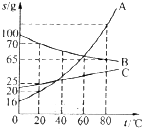
 �����ܽ�����ش��������⣺
�����ܽ�����ش��������⣺

 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
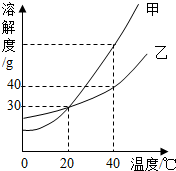 �ס��������ڲ�ͬ�¶��µ��ܽ����ͼ��ʾ��������ܽ�����ش��������⣺
�ס��������ڲ�ͬ�¶��µ��ܽ����ͼ��ʾ��������ܽ�����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
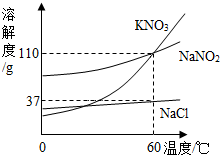 ��2013?��������ģ���������ƣ�NaNO2��������ʳƷ�ķ�ɫ���ͷ���������ʳƷ�е��������ƺ��������Σ�����彡�����������ƾ�����ζ�����κ�ʳ�κ����ƣ��������Ƶ�ˮ��Һ�ʼ��ԣ�������ҵ��������������ˮ�����Ӽ������������ڽ������ض�η������������Ƶ���ʳ��ʳ�õ����ж����¼���
��2013?��������ģ���������ƣ�NaNO2��������ʳƷ�ķ�ɫ���ͷ���������ʳƷ�е��������ƺ��������Σ�����彡�����������ƾ�����ζ�����κ�ʳ�κ����ƣ��������Ƶ�ˮ��Һ�ʼ��ԣ�������ҵ��������������ˮ�����Ӽ������������ڽ������ض�η������������Ƶ���ʳ��ʳ�õ����ж����¼����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
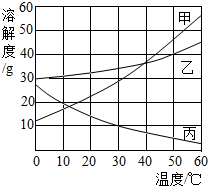 �ס��ҡ����������ʵ��ܽ��������ͼ��ʾ�������ܽ�����ش��й����⣺
�ס��ҡ����������ʵ��ܽ��������ͼ��ʾ�������ܽ�����ش��й����⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1���ڷǽ��������У�������ǿ�ķǽ������ѻ��������ķǽ�������Һ���û����������磺Cl2+2NaBr=Br2+2NaCl Br2+2NaI=I2+2NaBr I2+Na2S=S��+2NaI Cl2+2NaI=I2+2NaCl
��1���ڷǽ��������У�������ǿ�ķǽ������ѻ��������ķǽ�������Һ���û����������磺Cl2+2NaBr=Br2+2NaCl Br2+2NaI=I2+2NaBr I2+Na2S=S��+2NaI Cl2+2NaI=I2+2NaCl
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
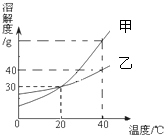 �ס��������ڲ�ͬ�¶��µ��ܽ����ͼ��ʾ��������ܽ�����ش��������⣺
�ס��������ڲ�ͬ�¶��µ��ܽ����ͼ��ʾ��������ܽ�����ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com