
分析 根据已有的金属的性质进行分析解答,验证金属活动性顺序可以依据金属能否与盐溶液反应进行.
解答 解:(1)生铁和钢都是含碳量不同的铁的合金,故填:铁;
(2)用铜作导线,主要利用铜具有良好的导电性,故填:导电;
(3)铝制品有良好的抗腐蚀性,其原因是在空气中铝的表面易形成致密的氧化铝薄膜,起到了保护作用,故填:氧化铝薄膜;
(4)A.Zn、Ag、CuCl2溶液,将锌放入氯化铜溶液中,能置换出铜,说明锌的活动性大于铜,将银放入氯化铜溶液中不富裕,说明铜大于银,正确;
B.Cu和Ag与ZnSO4溶液都不反应,说明锌在铜和银的前面,不能证明铜和银的活动性,错误;
C.Zn、Cu和AgNO3溶液都能反应,说明锌的和铜的活动性强于银,将锌放入铜和硝酸银反应生成的硝酸铜溶液中,有红色固体析出,说明锌大于铜,能证明金属的活动性,正确;
D.Zn能与稀硫酸反应,说明锌在氢的前面,Cu、Ag与稀硫酸都不反应,说明铜和银在氢的后面,不能证明铜和银的顺序,错误.
故填:AC.
点评 本题考查的是金属性质,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:选择题
| A. | 用pH试纸测溶液的酸碱度时,用手撕一条试纸再滴待测液 | |
| B. | 加热KClO3并用排水法收集O2实验结束时,先熄灭酒精灯,后移出导管 | |
| C. | 检查加热固体制气体装置气密性时,先手握试管再把导管伸入水中,观察是否有气泡 | |
| D. | 稀释浓硫酸时,先把水倒入烧杯中,后沿器壁缓慢注入浓硫酸,边加边用玻璃棒搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁钉在潮湿的空气中容易生锈,锈的主要成分是Fe3O4.xH2O | |
| B. | 可用燃着的火柴检查液化气罐是否泄漏 | |
| C. | 用铁锅烹饪会在食物中留有人体需要的铁元素 | |
| D. | 处理金属废弃物的方法是填埋法 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
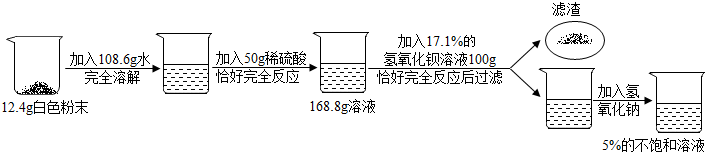
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
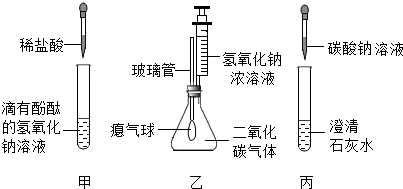
 请观察图丙根据图示回答下列问题.
请观察图丙根据图示回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
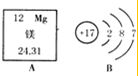
| A. | 表示一个二氧化硫分子 | B. | 由硫和氧气两种物质组成 | ||
| C. | 两种元素质量比为1:1 | D. | 硫元素的化合价为+4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钡溶液,静置 | 有白色沉淀,溶液无色 | 猜想1正确 |
| 若没有白色沉淀,溶液呈红色 | 猜想2正确 | |
| 有白色沉淀,溶液呈红色 | 猜想3正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com