
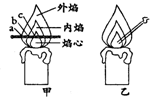
 »Æѧ¾ĶŌŚĪŅĆĒÉķ±ß£®Ö»ŅŖĪŅĆĒ²ÉČ”ŹŹµ±µÄŹµŃéŹÖ¶Ī£¬ĮōŠÄ¹Ū²ģ£¬¾ĶÄÜ“ÓĖ¾æÕ¼ū¹ßµÄŹĀĪļÖŠĪņ³öŗܶąæĘѧµĄĄķ£®ĮÕĮÕ¶ŌĄÆÖņ£ØÖ÷ŅŖ³É·ÖŹĒŹÆĄÆ£©¼°ĘäČ¼ÉÕ½ųŠŠĮĖČēĻĀĢ½¾æ£®£ØŅŃÖŖČ¼ÉÕ»į²śÉś¶žŃõ»ÆĢ¼£»¶žŃõ»ÆĢ¼ÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±ä³ÉŗģÉ«£©
»Æѧ¾ĶŌŚĪŅĆĒÉķ±ß£®Ö»ŅŖĪŅĆĒ²ÉČ”ŹŹµ±µÄŹµŃéŹÖ¶Ī£¬ĮōŠÄ¹Ū²ģ£¬¾ĶÄÜ“ÓĖ¾æÕ¼ū¹ßµÄŹĀĪļÖŠĪņ³öŗܶąæĘѧµĄĄķ£®ĮÕĮÕ¶ŌĄÆÖņ£ØÖ÷ŅŖ³É·ÖŹĒŹÆĄÆ£©¼°ĘäČ¼ÉÕ½ųŠŠĮĖČēĻĀĢ½¾æ£®£ØŅŃÖŖČ¼ÉÕ»į²śÉś¶žŃõ»ÆĢ¼£»¶žŃõ»ÆĢ¼ÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±ä³ÉŗģÉ«£©·ÖĪö ¢ń”¢¾ŻĻÖĻó·ÖĪö½ā“š£»
¢ņ”¢£Ø1£©øł¾Ż¶žŃõ»ÆĢ¼ÄÜÓėĖ®·“Ӧɜ³ÉĢ¼Ėį”¢Ģ¼ĖįæÉŹ¹ŹÆČļ±äŗģµÄŠŌÖŹÅŠ¶ĻŹĒŃéÖ¤ÄÄÖÖ¼ŁÉč¼“æÉ£»²»ÄÜµĆ³öÕżČ·µÄ½įĀŪŹĒŅņĪŖæÕĘųÖŠÓŠ¶žŃõ»ÆĢ¼£¬øÕ“µĆšµÄĄÆÖņÖÜĪ§ÉŠÓŠ²ŠÓąµÄĘäČ¼ÉÕÉś³ÉµÄ¶žŃõ»ÆĢ¼£»
£Ø2£©“µĆšĄÆÖņ£¬Į¢¼“ÓĆŅ»æéøɶųĄäµÄ²£Į§Ę¬·ÅŌŚ°×ŃĢÉĻ£¬²£Į§Ę¬ÉĻƻӊĖ®Īķ£¬ŹĒĪŖÖ¤Ć÷ŹĒ·ńŹĒĖ®ÕōĘų£»
£Ø3£©“µĆšĄÆÖņ£¬Į¢¼“Č¼×ŵÄľĢõČ„µć°×ŃĢ£Ø²»ŅŖ½Ó“„ÖņŠ¾£©£¬·¢ĻÖĄÆÖņÖŲŠĀ±»µćČ¼£¬ĖµĆ÷°×ŃĢ¾ßÓŠæÉČ¼ŠŌ£¬ŹĒĪŖ¼ŁÉč¢ŪĢį¹©ŅĄ¾Ż£»ÓÖŅņĪŖĖ®ÕōĘųŗĶ¶žŃõ»ÆĢ¼¶¼²»ÄÜČ¼ÉÕ£¬ĖłŅŌĶ¬Ź±æÉÅųż¼ŁÉč¢Ł¢Ś£¬¾Ż“ĖĶź³É½ā“š£®
½ā“š ½ā£ŗ¢ń”¢µćČ¼ĄÆÖņ£¬¹Ū²ģµ½»šŃę·ÖČż²ć£¬æÉŅŌ擵½»š²ń¹£µÄa“¦×īĻČĢ¼»Æ£¬ĖµĆ÷ĶāŃęµÄĪĀ¶Č×īøߣ¬
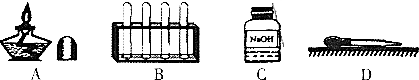
¢ņ”¢£Ø1£©¶žŃõ»ÆĢ¼ÄÜÓėĖ®·“Ӧɜ³ÉĢ¼Ėį”¢Ģ¼ĖįæÉŹ¹ŹÆČļ±äŗģ£¬“µĆšĄÆÖņĮ¢¼“ÓĆŅ»øöÕ“ÓŠ³ĪĒåŹÆ»ŅĖ®µÄÉÕ±ÕÖ×”°×ŃĢ£¬ĘäÄæµÄŹĒĪŖĮĖŃéÖ¤¼ŁÉčA”¢°×ŃĢŹĒČ¼ÉÕŹ±Éś³ÉµÄ¶žŃõ»ÆĢ¼£»µ«ÓÉÓŚøÕ“µĆšµÄĄÆÖņÖÜĪ§ÉŠÓŠ²ŠÓąµÄĘäČ¼ÉÕÉś³ÉµÄ¶žŃõ»ÆĢ¼£¬ĖłŅŌ²»ÄÜµĆ³öÕżČ·µÄ½įĀŪ£»
£Ø2£©“µĆšĄÆÖņ£¬Į¢¼“ÓĆŅ»æéøɶųĄäµÄ²£Į§Ę¬·ÅŌŚ°×ŃĢÉĻ£¬²£Į§Ę¬ÉĻƻӊĖ®Īķ£¬ĖµĆ÷°×ŃĢ²»ŹĒĖ®ÕōĘų£»
£Ø3£©“µĆšĄÆÖņ£¬Į¢¼“½«Č¼×ŵÄľĢõČ„µć°×ŃĢ£Ø²»ŅŖ½Ó“„ÖņŠ¾£©£¬·¢ĻÖĄÆÖņÖŲŠĀ±»µćČ¼£¬ĖµĆ÷°×ŃĢ¾ßÓŠæÉČ¼ŠŌ£¬Õā¾ĶÖ¤Ć÷ĮĖ¼ŁÉč¢ŪµÄÕżČ·ŠŌ£»ÓÖŅņĪŖĖ®ÕōĘųŗĶ¶žŃõ»ÆĢ¼¶¼²»ÄÜČ¼ÉÕ£¬ĖłŅŌĶ¬Ź±Ö¤Ć÷ĮĖ¼ŁÉč¢Ł¢ŚŹĒ²»ÕżČ·µÄ£»
¹Ź“š°øĪŖ£ŗ¢ń”¢a£»ĶāŃę£»
¢ņ”¢£Ø1£©¢Ł£»ĄÆÖņČ¼ÉÕŗóÄÜÉś³É¶žŃõ»ÆĢ¼£¬øÉČżģŃ飻
£Ø2£©Ė®ÕōĘų£»
£Ø3£©¢Ū£®
µćĘĄ ŹģĮ·ÕĘĪÕĪļÖŹµÄŠŌÖŹ£¬²¢ÄÜÉč¼ĘŹµŃé½ųŠŠŃéÖ¤£¬Ń§»įĢ½¾æĪŹĢāµÄŅ»°ć·½·Ø£¬ŅŖ½įŗĻĢāŅāĻøŠÄ·ÖĪö½ā“š£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| Ēā | Ńõ | Įņ | ĀČ | øĘ | Ģś | Ķ | He | Al | Ag |
| H | O | S | Cl | Ca | Fe | Cu | ŗ¤ | ĀĮ | Ņų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĪļÖŹ | ŅŅ“¼ | ŃõĘų | Ė® | ¶žŃõ»ÆĢ¼ | X |
| ·“Ó¦Ē°ÖŹĮæ/g | 4.6 | 8.0 | 0 | 0 | 0 |
| ·“Ó¦ŗóÖŹĮæ/g | 0 | 0 | 5.4 | 4.4 | a |
| A£® | ±ķÖŠaµÄÖµĪŖ2.6 | |
| B£® | XŅ»¶ØŹĒøĆ·“Ó¦µÄ“߻ƼĮ | |
| C£® | XæÉÄÜŗ¬ÓŠĒāŌŖĖŲ | |
| D£® | ČōĘšŹ¼Ź±ŃõĘųµÄÖŹĮæŹĒ10g£¬ŌņĪŽXÉś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö±šµ¹ČėÉŁĮæ³ĪĒåŹÆ»ŅĖ® | |
| B£® | ĪÅĘųĢåµÄĘųĪ¶ | |
| C£® | ·Ö±š½«Č¼×ŵÄľĢõÉģČėČżĘæĘųĢåÖŠ | |
| D£® | ·Ö±š½«“ų»šŠĒµÄľĢõÉģČėČżĘæĘųĢåÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com