
���� ��1������20��ʱ��NaCl���ܽ��Ϊ36g���з�����
��2�����ݻ�ѧ����ʽ�����е����ݽ��м��㣮
��� �⣺��1��20��ʱ��NaCl���ܽ��Ϊ36g�����Ա�����Һ�����ʺ��ܼ���������Ϊ��36g��100g=9��25��
��2��������H2������Ϊx������Cl2������Ϊy
2NaCl+2H2O�T2NaOH+H2��+Cl2��
117 2 71
36g��32.5% x y
$\frac{117}{36g��32.5%}=\frac{2}{x}=\frac{71}{y}$
x=0.2g
y=7.1g
ʣ����Һ������=136g?0.2g?7.1g=128.7g��
��ʣ����Һ������Ϊ128.7g��
�ʴ�Ϊ����1��9��25��
��2��ʣ����Һ������Ϊ128.7g��
���� ������Ҫ�����˻�ѧ����ʽ�ļ��㣬�ѶȲ���ע�����Ĺ淶�Ժ�ȷ�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
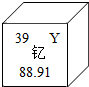 ����ѧ���Ļ�ѧ֪ʶ�ش��������⣮
����ѧ���Ļ�ѧ֪ʶ�ش��������⣮ �����ԭ���ڻ�ѧ��Ӧ�����õ����ӣ���õ�����ʧȥ������
�����ԭ���ڻ�ѧ��Ӧ�����õ����ӣ���õ�����ʧȥ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
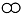 ���͡�
���͡� ���ֱ�������ֲ�ͬ�ĵ��ʷ���A2��B2��������һ���������ܷ�����ѧ��Ӧ���䷴Ӧ����ʾ��ͼ��ͼ��
���ֱ�������ֲ�ͬ�ĵ��ʷ���A2��B2��������һ���������ܷ�����ѧ��Ӧ���䷴Ӧ����ʾ��ͼ��ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����̼���ƺ��Ȼ��ƵĻ����Һ���μӹ������Ȼ�����Һ������ | |
| B�� | �Ʊ��������ƣ��������Ȼ�����Һ������������Һ��Ϻ���ˡ����� | |
| C�� | ��ȥCuSO4��Һ�е�H2SO4�����������Cu��OH��2������ | |
| D�� | �����������к���CO��CO2���Ƚ��������ͨ������������������ͭ�У���ͨ��ʯ��ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��˿����ʢ�����ļ���ƿ�о���ȼ�� | |
| B�� | �����ڿ�����ȼ�ղ����������� | |
| C�� | ��ȼ��ʱ�����д̼�����ζ������ | |
| D�� | ������������ˮʱ��Һ�¶Ƚ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
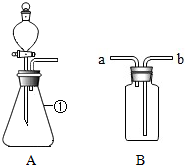 ͨ����һ��Ļ�ѧѧϰ�����Ѿ�������ʵ������ȡ������йط����������ͼ�ش����⣺
ͨ����һ��Ļ�ѧѧϰ�����Ѿ�������ʵ������ȡ������йط����������ͼ�ش����⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com