
| A. | 该反应是稀HCl滴入NaOH溶液 | |
| B. | a g是指加入氢氧化钠固体的质量 | |
| C. | A点溶液的溶质为HCl和NaCl | |
| D. | 检验B点溶液的溶质可先滴加足量的MgCl2,静置后再滴加少量AgNO3 |
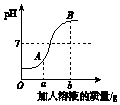
分析 A.从pH变化曲线图看,溶液的pH逐渐升高,说明是氢氧化钠溶液滴入稀盐酸中;
B.根据横轴的意义分析,ag是指加入氢氧化钠溶液的质量;
C.A点溶液显酸性,盐酸过量;
D.先滴加足量的MgCl2有白色沉淀生成,说明有氢氧化钠,且氢氧化钠被完全反应掉,静置后再滴加少量AgNO3溶液,有白色沉淀生成证明有氯化钠.
解答 解:A.从pH变化曲线图看,溶液的pH逐渐升高,说明是氢氧化钠溶液滴入盐酸,故错误;
B.ag是指加入氢氧化钠溶液的质量,故错误;
C.A点溶液显酸性,盐酸过量,因此A点溶液的溶质为HCl和生成的NaCl,故正确;
D.先滴加足量的MgCl2有白色沉淀生成,说明有氢氧化钠,且氢氧化钠被完全反应掉,静置后再滴加少量AgNO3溶液,有白色沉淀生成证明有氯化钠,故错误.
故选C.
点评 本题难度较大,掌握酸碱中和反应的过程以及氢氧化钠和氯化钠的性质是解题的关键.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:解答题
 某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出2克合金样品,每次加入稀硫酸10克,共加入稀硫酸4次,充分反应后,过滤、洗涤、干燥、称重,得到的实验数据如图所示:
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出2克合金样品,每次加入稀硫酸10克,共加入稀硫酸4次,充分反应后,过滤、洗涤、干燥、称重,得到的实验数据如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na+、Cl、SO42-、Fe3+ | B. | SO42-、NO3-、K+、H+ | ||
| C. | Ba2+、Cl-、CO32-、K+ | D. | Cl-、CO32-、K+、Na+ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 0℃ | 30℃ | 60℃ | 90℃ | |
| 甲 | 13.3克 | 45.8克 | 110克 | 202克 |
| 乙 | 35.5克 | 36.0克 | 37.1克 | 38.1克 |
| 丙 | 0.18克 | 0.16克 | 0.12克 | 0.08克 |
| A. | 降低温度可使丙的不饱和溶液变为饱和溶液 | |
| B. | 甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙 | |
| C. | 0℃时,三种物质的饱和溶液溶质质量分数甲>乙>丙 | |
| D. | 使乙物质从一定温度下的饱和溶液中析出,一般采用蒸发溶剂的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
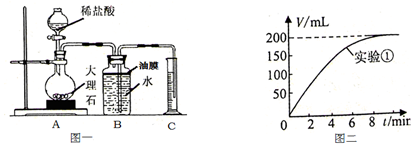
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
| 物质 | A | B | C | D |  |
| 分子示意图 |  |  |  |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com