
【题目】在一定条件下,甲、乙、两、丁四种物质在密闭容器中发生某个反应,测得反应前后各物质的质量如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 20 | 30 | 20 | 15 |
反应后质量/g | 0 | x | y | 10 |
下列叙述错误的的是( )
A.参加反应的甲与丁的质量比为4:1
B.x+y=75
C.y=20时,该反应一定是化合反应
D.x的取值范围:![]()
科目:初中化学 来源: 题型:
【题目】农业上常用质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如下图所示。
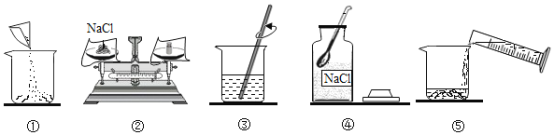
(1)实验操作顺序为_________。
(2)②中需称量NaCl的质量为_______。
(3)①中有部分固体洒落到烧杯外部,所得溶液的浓度_______(填“偏小”、“不变”或“偏大”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
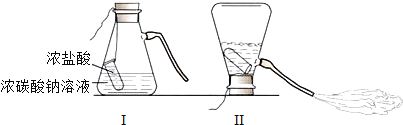
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是_____
(讨论与交流)
小明认为猜想1无需验证就知道是错误的,他的理由是___(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论_____(填“正确”或“错误”),理由是__。
(2)请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | 猜想3正确 |
(3)欲从猜想3的废液中得到纯净的NaCl晶体,请设计合理的实验方案_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组离子在pH=11的无色溶液中能大量共存的一组的是( )
A. Ca2+ 、Fe3+、Cl-、NO3-B. NH4+、Na+、SO42-、Cl-
C. Ba2+、K+、OH-、Cl-D. H +、Mg2+、HCO3-、NO3-
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是中学化学常见的化合物,其中B、C都是氧化物,D是一种碱,其相对分子质量为74,A、B、D、E属于不同类别的化合物。图中“-”表示相连的物质间能发生反应,“→”表示物质间存在转化关系。

(1)若A属于盐,则E属于______,C在生活中的一种用途是______。
(2)若A属于酸,则E生成B反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请据图回答下列问题:
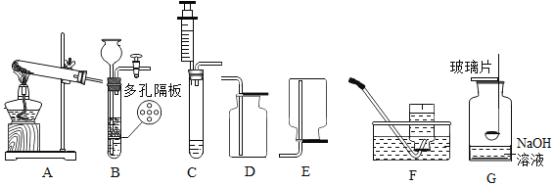
(1)若选用A装置作为在实验室制取氧气的发生装置,则制取氧气的化学反应方程式为______。
(2)实验室制取氧气,为了可以随时控制反应的发生与停止,应选择的发生装置是______![]() 填字母,下同
填字母,下同![]() ,收集装置为______。
,收集装置为______。
(3)用G装置做磷在氧气中燃烧试验,结束后取出燃烧匙,立即用玻璃片盖住瓶口并振荡,冷却后若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来,其原因是______。
(4)某化学兴趣小组拟对![]() 的性质进行探究,试验步骤如下:
的性质进行探究,试验步骤如下:
步骤1:如图甲、乙、丙三个气密性良好的烧瓶容积均为250mL,分别收集满![]() ,图中a处连接气体压力传感器,用于测定烧瓶内压力的变化,三个注射器内各装有85mL液体。
,图中a处连接气体压力传感器,用于测定烧瓶内压力的变化,三个注射器内各装有85mL液体。
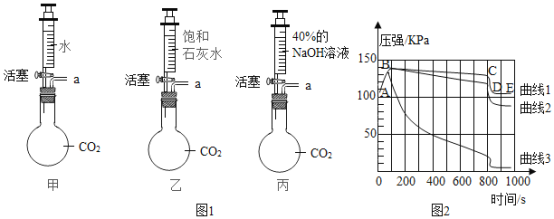
步骤2:三位同学同时迅速将注射器内液体全部注入各自烧瓶中,关闭活塞;一段时间后,同时振荡烧瓶。
步骤3:利用气体压力传感器测定烧瓶内从开始加入液体至振荡结束后的气压变化,得到如图2所示的压强与时间的关系曲线图,曲线1、2、3分别表示甲、乙、丙三个烧瓶内的气压变化。
①烧瓶丙中反应的化学方程式为______。
②曲线1中BC段气压逐渐变小的原因是______,导致CD段气压快速变小的操作是______。
③结合上述曲线2、3分析,除去![]() 气体选用氢氧化钠溶液而不选用石灰水,原因是______。
气体选用氢氧化钠溶液而不选用石灰水,原因是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属用途广泛,与我们的生活息息相关。请回答下列问题:
(1)常温下一些金属的物理性质数据如下:
金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
密度/(g﹒cm3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
熔点/°C | 1083 | 660 | 419 | 1535 | 328 |
硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
分析上述数据,碎石用的大锤常用铁制而不用铝制,原因是_____。
(2)铜器长期暴露在空气中,表面会生成铜绿[其成分可表示为Cu2(OH)2CO3],从其组成分析,预测铜绿能与_____,(任举一例)反应。
(3)铁生锈若不及时除去会加快生锈速度,写出实验室用硫酸除去铁锈的化学方程式_____。
(4)合金的很多性能与组成它们的纯金属不同。如图表示锡铅合金的是_____(填序号“a”“b”或“c”)。

(5)镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,它通常在真空中熔炼而非空气中熔炼,原因是_____(任写一个化学方程式)。
(6)2017年5月5日,我国首架大型客机C919试飞成功。该客机使用的多种新材料中有锂铝合金,锂铝合能用于制造飞机,说明它具有_____(填序号)的特点。
a、硬度大
b、密度小
c、易导电
d、耐腐蚀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明想测定部分变质的熟石灰样品中Ca(OH)2的质量分数,他称取0.5g该样品,加足量水使之充分溶解,搅拌过滤后,在滤液中加入10%盐酸溶液,加入盐酸溶液的质量和溶液的pH见表。
加入盐酸溶液的质量/g | 0 | 2.5 | 3.65 | 6 |
溶液的pH | 12 | 11 | 7 | 2 |
(1)当pH=2时,溶液中所含的溶质是_____(写化学式)。
(2)求样品中Ca(OH)2的质量分数_____。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )
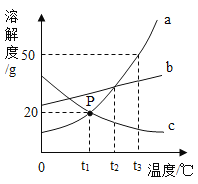
A. t1℃时,a、c两种物质饱和溶液的溶质质量分数为20%
B. 将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
C. 将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c
D. 将150g a物质的饱和溶液从t3℃降温至t1℃,可析出30g a物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com