
| A£® | SO42-”¢Cl-”¢Na+”¢OH- | B£® | K+”¢SO42-”¢Cu2+”¢Cl- | ||
| C£® | Ba2+”¢K+”¢SO42-”¢Na+ | D£® | NH4+”¢SO42-”¢Cl-”¢Na+ |
·ÖĪö øł¾ŻŠæµÄ»ī¶ÆŠŌĪ»ÓŚĒāÖ®Ē°£¬Ä³ĪŽÉ«ČÜŅŗÓėŠæ·“Ӧɜ³ÉĒāĘų£¬æÉÖŖøĆČÜŅŗÖŠ“ęŌŚ“óĮæµÄĒāĄė×Ó£¬½įŗĻø“·Ö½ā·“Ó¦·¢ÉśµÄĢõ¼žĄė×ÓÖ®¼äĮ½Į½½įŗĻ²»ÄܲśÉś³Įµķ”¢ĘųĢå»ņĖ®£¬æÉŅŌ“óĮæ¹²“ę£¬ĒŅ×¢ŅāČÜŅŗĪŖĪŽÉ«£®
½ā“š ½ā£ŗijĪŽÉ«ČÜŅŗÓėŠæ·“Ӧɜ³ÉĒāĘų£¬æÉÖŖøĆČÜŅŗÖŠ“ęŌŚ“óĮæµÄĒāĄė×Ó£¬Ņņ“Ė£ŗ
A”¢ĒāĄė×ÓŗĶĒāŃõøłĄė×Ó½įŗĻ²śÉśĖ®£¬²»Äܹ²“ę£¬¹ŹŃ”Ļī“ķĪó£»
B”¢ĖÄÖÖĄė×ÓÄܹ»ŌŚĖįŠŌĢõ¼žĻĀ¹²“ę£¬µ«ĶĄė×ÓĪŖĄ¶É«ČÜŅŗ£¬¹ŹŃ”Ļī“ķĪó£»
C”¢ĮņĖįøłĄė×ÓŗĶ±µĄė×Ó½įŗĻ²śÉśĮņĖį±µ³Įµķ£¬²»Äܹ²“ę£¬¹ŹŃ”Ļī“ķĪó£»
D”¢ĖÄÖÖĄė×ÓÄܹ»ŌŚĖįŠŌĢõ¼žĻĀ¹²“ę£¬ĒŅ²»“ęŌŚ“ųÉ«µÄĄė×Ó£¬¹ŹŃ”ĻīÕżČ·£»
¹ŹŃ”ĻīĪŖ£ŗD£®
µćĘĄ ŌŚ½āÕāĄąĢāŹ±Ź×ĻČøł¾ŻĢāÖŠµÄĢõ¼ž£¬ÅŠ¶Ļ³öČÜŅŗÖŠ“ęŌŚµÄĄė×Ó£¬Č»ŗóŌŁÓėø÷øöŃ”Ļī¶Ō½Ó£¬Ö»ŅŖ»įÉś³É³Įµķ”¢ĘųĢ唢Ė®ÖŠµÄŅ»ÖÖ£¬¾Ķ²»Äܹ²“ę£¬×¢ŅāĪŽÉ«ČÜŅŗÖŠ²»ÄÜÓŠ“ųÉ«µÄĄė×Ó“ęŌŚ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
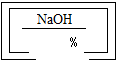 Š”ĘęĶ¬Ń§ŌŚŹµŃéŹŅ·¢ĻÖÓŠŅ»Ęæ±źĒ©²ŠČ±£ØČēĶ¼ĖłŹ¾£©µÄNaOHČÜŅŗ£®ĪŖĮĖČ·¶Ø“ĖČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹż£¬ĖūČ”ÓĆ50g“ĖNaOHČÜŅŗ£¬ĀżĀżµĪ¼ÓŅ»¶ØÅØ¶ČµÄĮņĖįĶČÜŅŗÖĮ²»ŌŁ²śÉś³ĮµķĪŖÖ¹£¬¹²ĻūŗÄĮņĖįĶČÜŅŗ100g£¬¹żĀĖ£¬µĆµ½ĀĖŅŗ145.1g£®ŹŌ¼ĘĖć
Š”ĘęĶ¬Ń§ŌŚŹµŃéŹŅ·¢ĻÖÓŠŅ»Ęæ±źĒ©²ŠČ±£ØČēĶ¼ĖłŹ¾£©µÄNaOHČÜŅŗ£®ĪŖĮĖČ·¶Ø“ĖČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹż£¬ĖūČ”ÓĆ50g“ĖNaOHČÜŅŗ£¬ĀżĀżµĪ¼ÓŅ»¶ØÅØ¶ČµÄĮņĖįĶČÜŅŗÖĮ²»ŌŁ²śÉś³ĮµķĪŖÖ¹£¬¹²ĻūŗÄĮņĖįĶČÜŅŗ100g£¬¹żĀĖ£¬µĆµ½ĀĖŅŗ145.1g£®ŹŌ¼ĘĖć²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øɱłÓĆ×÷ÖĘĄä¼Į-øɱłŹĒ±ł | |
| B£® | ÓĆĢæŗŚÄ«ÖŹéŠ“µÄ×Ö¾¾Ć²»±äÉ«-³£ĪĀĻĀ£¬Ģ¼µÄ»ÆѧŠŌÖŹĪČ¶Ø | |
| C£® | “æ¼īČÜŅŗŹ¹·ÓĢŖ±äŗģ-“æ¼īŹĒ¼ī | |
| D£® | ÖĘĢĒ¹¤ŅµÓĆ»īŠŌĢæĶŃÉ«ÖĘ°×ĢĒ-»īŠŌĢæŗĶÓŠÉ«ĪļÖŹ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŠņŗÅ | “ż¼ų±šµÄĪļÖŹ | ¼ų±šŹŌ¼Į»ņ·½·Ø |
| A | ŃņĆ«ÓėŗĻ³ÉĻĖĪ¬ | ×ĘÉÕ£¬ĪÅĘųĪ¶ |
| B | ĻõĖįļ§ÓėŹ³ŃĪ¹ĢĢå | Ė® |
| C | ĒāŃõ»ÆÄĘČÜŅŗÓėĢ¼ĖįÄĘČÜŅŗ | ·ÓĢŖČÜŅŗ |
| D | Ņ»Ńõ»ÆĢ¼Óė¶žŃõ»ÆĢ¼ĘųĢå | ³ĪĒåµÄŹÆ»ŅĖ® |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ŅņĪŖCO2ÄÜČÜÓŚĖ®£¬ĖłŅŌ²»ÄÜÓĆÅÅĖ®·ØŹÕ¼Æ | |
| B£® | ÓĆÅÅĖ®·ØæÉŅŌÖ±½ÓŹÕ¼Æµ½“æ¾»ĒŅøÉŌļµÄĒāĘų | |
| C£® | ŅņĪŖ³£ĪĀŹ±NOŗĶO2·“Ӧɜ³ÉNO2£¬ĖłŅŌ²»ÄÜÓĆÅÅæÕĘų·ØŹÕ¼ÆNO | |
| D£® | ŅņĪŖCOÓŠ¶¾£¬ĖłŅŌ²»ÄÜÓĆÅÅæÕĘų·ØŹÕ¼Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
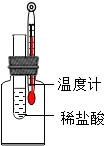 Ķ¼ĖłŹ¾×°ÖĆĘųĆÜŠŌĮ¼ŗĆ£¬ŹŌ¹Ü֊װӊĻ”ŃĪĖį£®ĻņŹŌ¹ÜÖŠ¼ÓČėijĪļÖŹŗó£¬ĪĀ¶Č¼ĘĪĀ¶ČÉżøߣ¬øĆĪļÖŹŹĒ£Ø””””£©
Ķ¼ĖłŹ¾×°ÖĆĘųĆÜŠŌĮ¼ŗĆ£¬ŹŌ¹Ü֊װӊĻ”ŃĪĖį£®ĻņŹŌ¹ÜÖŠ¼ÓČėijĪļÖŹŗó£¬ĪĀ¶Č¼ĘĪĀ¶ČÉżøߣ¬øĆĪļÖŹŹĒ£Ø””””£©| A£® | Ć¾“ų | B£® | ±łæé | C£® | Ķæé | D£® | ĀČ»ÆÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com