
【题目】将5%的NaOH溶液逐滴加入到10g稀硫酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答: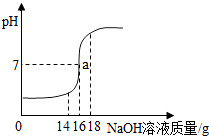
(1)a点的含义是;
(2)当计入NaOH溶液的质量为18g时,溶液中存在的阴离子有;
(3)计算稀硫酸中溶质的质量分数.
【答案】
(1)当加入NaOH溶液的质量为16g时,硫酸与氢氧化钠恰好完全中和
(2)硫酸根离子与氢氧根离子
(3)解:设10g稀硫酸中溶质的质量为x,则
H2SO4+ | 2NaOH=Na2SO4+2H2O |
98 | 80 |
x | 16g×5% |
![]() =
=![]() ,得x=0.98g
,得x=0.98g
稀硫酸中溶质的质量分数=![]() ×100%=9.8%.
×100%=9.8%.
答:稀硫酸中溶质的质量分数为9.8%.
【解析】解:(1)a点的含义是:当加入NaOH溶液的质量为16g时,硫酸与氢氧化钠恰好完全中和.
故填:当加入NaOH溶液的质量为16g时,硫酸与氢氧化钠恰好完全中和.
(2)当计入NaOH溶液的质量为18g时,氢氧化钠过量,此时溶液中存在的阴离子有硫酸根离子与氢氧根离子.
故填:硫酸根离子与氢氧根离子.
(3)设10g稀硫酸中硫酸质量为x,
H2SO4+2NaOH═Na2SO4+2H2O
98 80
x 16g×5%
![]() =
=![]()
x=0.98g
稀硫酸中溶质的质量分数=![]() ×100%=9.8%.
×100%=9.8%.
答:稀硫酸中溶质的质量分数为9.8%.
所以答案是:(1)当加入NaOH溶液的质量为16g时,硫酸与氢氧化钠恰好完全中和;(2)硫酸根离子与氢氧根离子;(3)9.8%.
【考点精析】掌握根据化学反应方程式的计算是解答本题的根本,需要知道各物质间质量比=系数×相对分子质量之比.


科目:初中化学 来源: 题型:
【题目】化学方程式是学习化学的重要工具之一。根据化学方程式不能获得的信息是( )。
A. 该反应中的反应物和生成物 B. 化学反应的快慢
C. 各反应物和生成物的质量比 D. 参加反应的各粒子的相对数量关系
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类法是化学学习的重要方法,下列各组物质按单质、氧化物、混合物的顺序排列的是( )
A. 水银、冰水混合物、天然气 B. 液氧、氯化钙、大理石
C. 水、碳酸钙、海水 D. 空气、氧化铜、碘酒
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用科学方法去探究
科学方法是人们在认识和改造客观世界的实践中总结出来的正确的思维和行为方式,是科学研究与解决问题过程中所采用的方法、途径和手段。观察、比较、分类、类比、归纳等是我们化学学习中经常用到的科学方法。
A.观察是有目的、有计划对客观事物的主动感受和知觉。
B.比较是确定对象之间差异点和共同点的方法。
C.分类是根据对象的共同点和差异点,将对象区分为不同种类的方法。
D.类比是根据两个或两类对象之间在某些方面相似或相同,从而推出它们在其他方面也可能相同或相似的方法。
e.归纳是从个别事物的性质、特点和关系中概括出一类事物的性质、特点和关系的方法。
小华在探究盐酸能与哪些物质发生化学反应时,进行了如下图所示的实验:
(1)在他的实验记录里的如下五个陈述中,请说出每个陈述分别是运用了上述哪一种科学方法? (在答题纸相应的位置填编号)
①选择的物质中紫色石蕊属于酸碱指示剂、镁和铁属于金属单质、碳酸钠和硝酸银属于盐、铁锈属于金属氧化物。
②镁条与稀盐酸作用产生大量的气泡,试管壁发热。
③镁条与盐酸的反应比铁片与盐酸反应激烈。
④活泼的金属单质与稀盐酸发生的化学反应都属于放热的化学反应。
⑤氧化铜和氧化铁都属于金属氧化物,因此氧化铜也可以与稀盐酸发生反应。
(2)写出有关反应的化学方程式:
①铁片与稀盐酸;
②铁锈与稀盐酸。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙的溶解度曲线如下图所示,将t2℃甲、乙的饱和溶液分别降温到t1℃时。下列说法一定正确的是( )
A.两溶液仍饱和
B.甲溶液仍饱和
C.溶质质量分数:甲=乙
D.溶液质量:甲=乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】使用图装置可以进行下列实验中的( )
A.锌与稀硫酸制取、收集氢气
B.石灰石与稀硫酸制取、收集二氧化碳
C.KMnO4制取、收集氧气
D.过氧化氢溶液与MnO2制取、收集氧气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com