某钢铁厂购进含氧化铁(Fe2O3)85%的赤铁矿1000t,计算用这些铁矿石可炼取含杂质3%的生铁多少吨?(计算结果保留整数)
【答案】
分析:工业冶炼生铁的原理反应为Fe
2O
3+3CO

2Fe+3CO
2,根据反应的化学方程式确定氧化铁与铁的质量关系,再利用矿石中氧化铁的质量计算可冶炼得生铁的质量.
解答:解:设1000t含氧化铁85%的赤铁矿可炼取含杂质3%的生铁的质量为x.则
Fe
2O
3+3CO
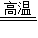
2Fe+3CO
2
160 112
1000t×85% x×(1-3%)
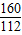
=

,
解得,x=613t
答:用这些铁矿石可炼取含杂质3%的生铁613吨.
(注:设不正确、计算过程不带单位,共扣(1分).)
点评:在使用化学方程式进行计算时,代入化学方程式的量一定是纯净物的质量,不能把混合物的质量直接代入化学方程式进行计算.
