
【题目】下图为a、b、 c三种物质的溶解度曲线
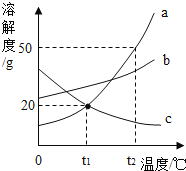
(1)t2°C时,a、b、c三种物质的溶解度由大到小的顺序是_______________。
(2)t1°C时,a、c饱和溶液的溶质质量分数_______________。 (填 “相等”或“不相等”);
(3)将c的饱和溶液变为不饱和溶液,除增加溶剂外,还可采取____的方法;
(4)t2°C时,将a物质30g放入50g水中,充分溶解,所得溶液中,溶质和溶液的质量比为___________;若保持温度不变,向溶液中再加入10g水,充分溶解后, 溶液的溶质质量分数_________ (填“变大”、“变小”或“不变”)。
(5)某溶液在室温下蒸发5g水析出ng晶体,再蒸发5g水又析出mg晶体,则n与m______相等(填“一定”或“不一定”)。
【答案】a>b>c 相等 降低温度 1:3 不变 不一定
【解析】
(1)由曲线图可知,t2°C时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c。
(2)由曲线图可知,t1°C时,a、c饱和溶液的溶解度相等,根据溶质质量分数![]() ,故t1°C时,a、c饱和溶液的溶质质量分数相等。
,故t1°C时,a、c饱和溶液的溶质质量分数相等。
(3)由曲线图可知,c物质的溶解度随温度的升高而减小,将c的饱和溶液变为不饱和溶液,除增加溶剂外,还可采取降低温度的方法。
(4)已知在t2°C时,a物质的溶解度为50g,将a物质30g放入50g水中,最多能溶解a物质25g,所得溶液为饱和溶液,溶质和溶液的质量比为25g:75g=1:3;若保持温度不变,向溶液中再加入10g水,则60g水刚好能溶解a物质30g,所得溶液为饱和溶液, 故溶液的溶质质量分数不变。
(5)某溶液在室温下蒸发5g水析出ng晶体,再蒸发5g水又析出mg晶体,则n与m不一定相等。因为第一次蒸发前溶液不一定是饱和溶液,而第二次蒸发前溶液为饱和溶液,故无法确定n与m是否相等。


科目:初中化学 来源: 题型:
【题目】向一定量盐酸和氯化铁溶液的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
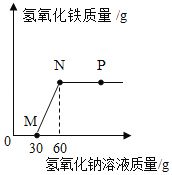
A. P点表示的溶液中只含有一种溶质
B. N点表示的溶液pH=7
C. P点和N点表示的溶液中,NaC1的质量分数相同
D. 从M点到N点溶液质量增加30g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究碳与氧化铜反应的气体产物中是否有一氧化碳,某同学进行如下实验过程。(装置B和D内均是足量澄清石灰水)

①A处加热一段时间后,试管中的现象是_______。
②B处石灰水变浑浊,其反应的化学方程式是______,
③若能说明A处反应的气体产物中有一氧化碳,依据的一个现象是_____。
为进一步确定碳与氧化铜反应产生一氧化碳的质量,该同学测量了如下数据:
A处 试管内物质 | B处 瓶内物质 | C处 玻璃管内物质 | D处 瓶内物质 | |
反应前后质量变化量 (g) | a | b | c | d |
则一氧化碳的质量m(CO)=____________。(用上述字母表达)
④停止实验,待C处玻璃管冷却,倒出固体于试管中,加入足量稀硫酸,看到____现象,则推出固体的成分是氧化铜和铜。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以化合价为纵坐标,所绘制的图象叫价类图。如图是以物质的类别为横坐标,以硫元素化合价纵坐标绘制的硫的价类图。例如E点可表示硫酸钡,其中S为+6价。请回答下列问题:

(1)A点对应物质的类别是___;
(2)带两个单位负电荷的硫离子的结构示意图为___;
(3)在工业上,煅烧黄铁矿的化学方程式为4FeS2+11O2![]() 2Fe2O3+8X,则生成物X化学式为___,标出黄铁矿的主要成分 FeS2(二硫化亚铁)中硫元素的化合价___,工业上用含此反应产物的矿石进行炼铁的设备叫做___;
2Fe2O3+8X,则生成物X化学式为___,标出黄铁矿的主要成分 FeS2(二硫化亚铁)中硫元素的化合价___,工业上用含此反应产物的矿石进行炼铁的设备叫做___;
(4)用化学方程式完成任意一条酸雨的形成途径___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学进行了如下实验,验证一氧化碳与氧化铜的反应
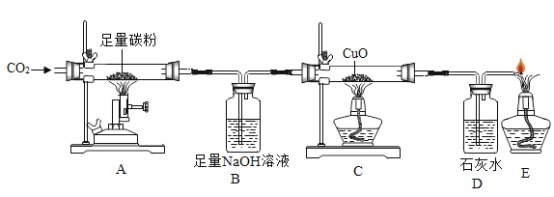
①进入装置 B 的气体中含有二氧化碳和_____
②C 处氧化铜发生反应的化学方程式是_____;D 中观察到的现象是______
③对于该实验的相关分析,正确的是_____(选填编号)
a 实验开始时,先缓慢通入二氧化碳,D 中无明显现象
b 装置 B 中无明显现象,说明该装置中没有发生反应
c 装置 E 的作用是将尾气点燃,防止污染空气
d 实验结束后,装置 C 玻璃管中固体减少的质量等于装置 D 中增加的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某碳酸氢钠中含有少量的氯化铵,为测得碳酸氢钠的含量设计以下两个方案![]() 已知:碳酸氢钠与碱反应生成碳酸钠
已知:碳酸氢钠与碱反应生成碳酸钠![]()
方案一:取样品mg,滴加足量稀盐酸,收集生成的气体ng。
方案二:取样品mg,滴加硝酸酸化的硝酸银溶液,生成沉淀的质量为zg。
(1)方案一中发生反应的化学方程式是______。
(2)下列说法正确的是______
A 加入硝酸的目的是除去碳酸氢钠
B 可以用稀盐酸代替稀硝酸
C 反应生成的沉淀要经过洗涤,干燥
(3)同学们经过讨论认为通过其他两条途径也可以达到目的,方案是取品mg加入足量氢氧化钠溶液,①测收集到的______(填化学式)质量;②加入过量的______溶液后测生成沉淀的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】5G商用加速推出,“中国芯”崛起,“中国创造”绽放异彩!芯片的主要成分是纯度极高的硅,如图为硅在元素周期表中的部分信息,下列说法错误的是
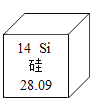
A.硅元素属于金属元素
B.硅原子的核电荷数是14
C.硅原子的核外电子数为14
D.硅的相对原子质量为28.09
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Ca(OH)2 和NaOH是重要的碱。在不同温度时的溶解度如下:
温度(°C) | 20 | 40 | 60 | 80 | |
溶解度(g/100g 水) | Ca(OH)2 | 0.17 | 0.14 | 0.09 | 0.08 |
NaOH | 109 | 129 | 174 | 314 | |
①20°C时Ca(OH)2的溶解度是_________。
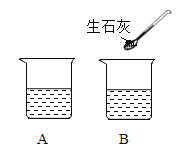
②A、B二只烧杯装有等质量的饱和石灰水(如图所示)。B烧杯中加入少量生石灰,写出发生反应的化学方程式___________。此时,A、B烧杯中溶液质量A__________B (选填“>”、“<”或“=”)。
③20°C时100g饱和NaOH溶液蒸发10g水后,恢复到原温度,析出___________gNaOH固体。
④60°C时NaOH饱和溶液中含少量Ca(OH)2,若要得到较纯净NaOH晶体,应采取的物理方法是________。
⑤若在20°C时,鉴别Ca(OH)2、NaOH饱和溶液,可选用的方法是_____________。
I 降低温度
II 滴加酚酞溶液
III 测pH
IV 滴入盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com