
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.10 | 8.45 | 7.80 | 7.80 |
分析 由表中数据可知,第二次和第三次反应的锌的质量都是0.65g,则第一次反应的锌质量也是0.65g,因此可以计算黄铜样品的质量,进一步可以计算黄铜样品中铜的质量分数;
根据第一次、第二次、第三次数据都可以计算所用稀盐酸中溶质的质量分数.
解答 解:(1)因为第一次、第二次、第三次反应的锌质量都是0.65g,则样品质量为:9.10g+0.65g=9.75g,
黄铜样品中铜的质量分数为:$\frac{7.80g}{9.75g}$×100%=80%,
故填:80%.
(2)设10g稀盐酸中氯化氢质量为x,
Zn+2HCl═ZnCl2+H2↑,
65 73
0.65g x
$\frac{65}{0.65g}$=$\frac{73}{x}$,
x=0.73g,
所用稀盐酸中溶质的质量分数为:$\frac{0.73g}{10g}$×100%=7.3%,
答:所用稀盐酸中溶质的质量分数是7.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:选择题
| A. | 莽草酸是由22个原子构成的化合物 | |
| B. | 莽草酸中氢元素的质量分数最高 | |
| C. | 莽草酸是由碳,氢,氧三种元素组成的 | |
| D. | 莽草酸的相对分子质量是174克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气中含量最多的气体是氧气 | B. | 空气由氮元素、氧元素组成 | ||
| C. | 大雨过后洁净的空气是混合物 | D. | 空气中的各种气体成分都是单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 物质(括号内为杂质) | 除杂试剂 |
| A | CO(CO2) | 碱石灰(CaO和NaOH混合物) |
| B | CaCl2溶液(HCl) | Ba(OH)2溶液 |
| C | C(CuO) | 盐酸 |
| D | NaOH溶液[Ca(OH)2] | NaNO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
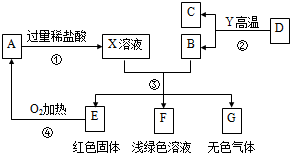
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
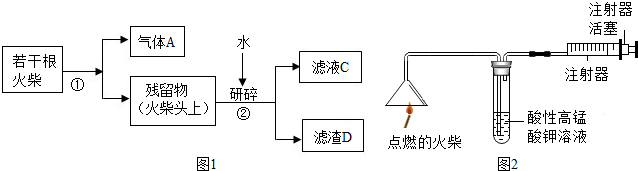
| 实验次序 | H2O2溶液的质量分数 | H2O2溶液 用量/毫升 | 物质D 用量/克 | 反应温度/℃ | 收集气体 体积/毫升 | 所需时间/秒 |
| ① | 0.30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 0.15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 0.15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 0.5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 0.30 | 5 | 0 | 55 | 2 | 10.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com