
【题目】二氧化钛(Ti02 )可作水分解的光催化剂.二氧化钛中钛元素的化合价为( )
A.+1 B.+2 C.+3 D.+4
科目:初中化学 来源: 题型:
【题目】(8分)有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。
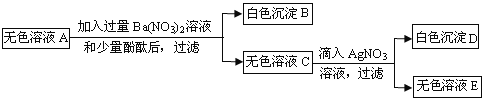
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如下图所示的实验。
请回答下列问题:
(1)B的化学式是 。
(2)A中一定存在的溶质的化学式是 。
(3)生成白色沉淀D的化学方程式是 。
(4)这包粉末中可能含有物质的化学式是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】发生地震后,为了灾区防疫,会使用过氧乙酸(C2H4O3)消毒液进行环境消毒,下列说法正确的是
A.过氧乙酸是氧化物
B.过氧乙酸中碳、氢、氧元素的原子个数比为2:4:3
C.过氧乙酸由9个原子构成
D.过氧乙酸的相对分子质量为76g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A.太阳能、核能、风能等是值得开发和利用的新能源
B.空气是一种宝贵的资源,其中含量最多的是氧气
C.海水淡化只能得到淡水,剩余物不再有利用价值
D.人类利用的能量都是通过化学反应获得的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)已知CO2通入澄清石灰水中,溶液变浑浊,继续通CO2气体由浑浊又变澄清,CaCO3+H2O+CO2 = Ca(HCO3)2,由此某化学兴趣小组欲探究CO2与NaOH溶液反应后的溶质组成。
【提出问题】CO2与NaOH溶液反应后的溶质组成
【查阅资料】1、NaHCO3+NaOH===Na2CO3+H2O
2、盐酸滴入碳酸钠溶液中,实际反应分两步进行
第一步反应:Na2CO3+HCl=NaCl+ NaHCO3
第二步反应:NaHCO3+HCl=NaCl+ H2O+CO2↑
【提出猜想】猜想1:溶质为Na2CO3
猜想2:溶质为 (填化学式,以下同)
猜想3:溶质为
猜想4:溶质为
【实验方案】I甲组同学为确定CO2与NaOH溶液反应后所得溶液中溶质组成,设计如下实验方案。
(1)向所得溶液中加入足量的CaCl2溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸无气泡产生,则溶质为 。
(2)向所得溶液中加入足量的CaCl2溶液,若无白色沉淀生成,溶液中加入足量的稀盐酸有气泡产生,则溶质为 。
(3)向所得溶液中加入足量的CaCl2溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸有气泡产生,则溶质为 。
II乙组同学根据甲组同学的猜想,通过定量分析绘制出向所得溶液中逐滴加入稀盐酸的质量与生成二氧化碳的质量关系示意图,请根据图像确定溶质成分。
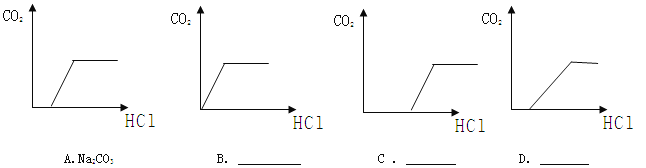
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有①石油 ②石墨 ③矿泉水 ④铁 ⑤氯酸钾 ⑥干冰。
对上述物质的分类正确的是
A.混合物——①②③ B.氧化物——⑤⑥
C.单质——②④ D.化合物——③⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)阅读下面科普短文(原文作者:段翰英等)。
我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐[如亚硝酸钠(![]() )]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(![]() )和氯化物(如
)和氯化物(如![]() )。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?含量有多少?含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。
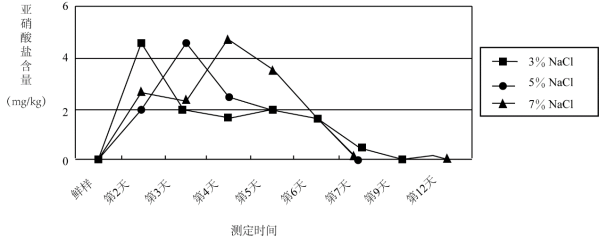
用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由 转化成生的。
(2)亚硝酸钠能与盐酸反应,该反应属于基本反应类型中的 反应。
(3)室温下,用芹菜制作的泡菜,最佳食用时间是 (填字母序号,下同)。
A.泡制2-3天 B.泡制5-6天 C.泡制12天后
(4)下列关于制作泡菜的说法中,合理的是 。
A.最好加入一些姜汁
B.最好在较低温度下泡制
C.最好加入一些富含维生素C的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(5)请你为喜欢吃泡菜的人提一条食用泡菜的建议: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(14分)连云港碱厂年产纯碱120万吨,是我国三大纯碱生产企业之一。它的产品除了纯碱外,还有氯化钙和碳酸氢钠。该厂生产纯碱的工艺流程可简单表示如下:
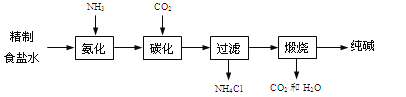
其生产过程中涉及的主要化学反应有:
①NaCl + NH3 + CO2 + H2O = NH4Cl + NaHCO3↓
②2NaHCO3![]() Na2CO3+ CO2↑+ H2O
Na2CO3+ CO2↑+ H2O
请回答:
(1)①“碳化”过程中需要的CO2,可由石灰石高温煅烧得到,该反应的化学方程式为 。
②实验室中,通常用稀盐酸与石灰石反应制取CO2气体,不选用浓盐酸的理由是 ;干燥CO2气体,可用的干燥剂是 (填字母)。
A.浓硫酸 B.固体氢氧化钠 C.生石灰
(2)①该厂“过滤”所得的NH4Cl可作化肥中的 肥,它也可与Ca(OH)2在加热时发生反应生成产品CaCl2,同时还有NH3和H2O生成,写出该反应的化学方程式: 。
该厂的另一种产品碳酸氢钠俗称 ,它的重要用途有 (只写一种)。
②实验室进行“过滤”操作时,下列说法正确的有 (填字母)
A.使用的漏斗叫长颈漏斗 B.液面应低于滤纸边缘
C.玻璃棒应不停搅拌 D.漏斗下端的管口要紧靠烧杯内壁
(3)某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案:
方案一:称取样品10.65g,加水完全溶解,向其中加入足量的氯化钡溶液,充分反应后,过滤、洗涤,干燥得固体19.70g。通过计算(写出计算过程)判断该厂的产品是否属于优等品 。(杂质可溶于水且不与氯化钡反应)
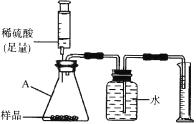
方案二:用下图所示的装置,通过准确测量排出水的体积,也可计算样品的纯度。该装置中仪器A的名称是 ,但实验后同学们发现所测的碳酸钠的纯度偏低,造成此结果的原因可能是 。(装置的气密性良好)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com