
ŹµŃéŹŅ²æ·ÖŅĒĘ÷»ņ×°ÖĆČēĶ¼ĖłŹ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā”£





| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗÓÄĻŹ”ŌĆūŠ£2018½ģ¾ÅÄź¼¶æ¼µŚĖÄ“Ī“óĮŖæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĶ¼Ļń²»ÄÜÕżČ··“Ó³Ęä¶ŌÓ¦¹ŲĻµµÄŹĒ

A. µČÖŹĮæµÄĆ¾·ŪŗĶŠæ·ŪÓė×ćĮæČÜÖŹÖŹĮæ·ÖŹżĻąĶ¬µÄĻ”ĮņĖį·“Ó¦
B. ±£³ÖĪĀ¶Č²»±ä£¬ĻņŅ»¶ØĮæµÄ±„ŗĶŹÆ»ŅĖ®ÖŠ¼ÓČĖŃõ»ÆøĘ
C. ³ØæŚ·ÅÖƵÄŅ»¶ØĮæÅØĮņĖį
D. ĻņŅ»¶ØĮæŗ¬ÓŠĻ”ŃĪĖįŗĶĮņĖįĶµÄ»ģŗĻČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ
B ”¾½āĪö”æA. Ć¾µÄ»ī¶ÆŠŌ±ČŠæµÄĒ棬ĖłŅŌĆ¾ĻČ·“Ó¦Ķź£¬µČÖŹĮæµÄĆ¾·ŪŗĶŠæ·ŪÓė×ćĮæČÜÖŹÖŹĮæ·ÖŹżĻąĶ¬µÄĻ”ĮņĖį·“Ó¦£¬×īÖÕĆ¾ŗĶŠæ¶¼ĶźČ«·“Ó¦£¬Ć¾±ČµČÖŹĮæµÄŠæÉś³ÉĒāĘų¶ą£¬ÕżČ·£»B. ±£³ÖĪĀ¶Č²»±ä£¬ĻņŅ»¶ØĮæµÄ±„ŗĶŹÆ»ŅĖ®ÖŠ¼ÓČĖŃõ»ÆøĘ£¬Ńõ»ÆøĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘ£¬ČܼĮ¼õÉŁ£¬Ķ¬Ź±ÓÉÓŚČܼĮ¼õÉŁµ¼ÖĀČÜÖŹĪö³ö£¬ČÜÖŹŅ²¼õÉŁ£¬ĖłŅŌČÜŅŗµÄÖŹĮæ¼õÉŁ£¬“ķĪó£»C. ³ØæŚ·ÅÖƵÄŅ»¶ØĮæÅØĮņĖį£¬ŅņĪüĖ®ČܼĮŌö¶ą£¬ČÜÖŹ²»±ä£¬ČÜŅŗµÄÖŹĮæŌö¼Ó£¬...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗĻĆĆÅŹŠĻč°²Ēų2018½ģ¾ÅÄź¼¶ÖŠæ¼ø“Ļ°Ä£Äā¾ķ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ¶ąŃ”Ģā
(Ė«Ń”)ĻÖÓŠŠæŗĶĮķŅ»ÖÖ½šŹō×é³ÉµÄ»ģŗĻĪļ£¬°Ń6.5 gøĆ»ģŗĻĪļ¼ÓČėµ½100 gŅ»¶ØČÜÖŹÖŹĮæ·ÖŹżµÄĻ”ĮņĖįÖŠ£¬Ē”ŗĆĶźČ«·“Ó¦£¬²śÉśĒāĘųµÄÖŹĮæĪŖw”£ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)
A. Čō»ģŗĻĪļĪŖZn”¢Al£¬wæÉÄÜŹĒ0.2 g
B. Čō»ģŗĻĪļĪŖZn”¢Fe£¬w²»æÉÄÜŹĒ0.2 g
C. Čō»ģŗĻĪļĪŖZn”¢Cu£¬wŹĒ0.1 g£¬ŌņøĆ»ģŗĻĪļÖŠŠæµÄÖŹĮæ·ÖŹżĪŖ50%
D. Čō»ģŗĻĪļĪŖZn”¢Mg£¬Ōņ¼ÓČėµÄĻ”ĮņĖįÖŠČÜÖŹÖŹĮæ·ÖŹżŅ»¶Ø“óÓŚ10%
BC ”¾½āĪö”æ¼ŁÉč6.5gČ«²æĪŖŠæ£¬ÉčÉś³ÉĒāĘųÖŹĮæĪŖx£¬Ōņ£ŗ Zn+H2SO4ØTZnSO4+H2”ü 65 98 2 6.5g y x ½āµĆx=0.2g£»y=9.8g Ķ¬ĄķæɼĘĖć³ö6.5gĀĮ”¢ĢśÓė×ćĮæĮņĖį·“Ó¦²śÉśĒāĘųµÄÖŹĮæ“óÓŚ0.2g”£A. Čō»ģŗĻĪļĪŖZn”¢Al£¬w“óÓŚ0.2 g£¬“ķĪó£»B”¢B. Čō»ģŗĻĪļĪŖZn”¢Fe£¬w“óÓŚ0.2 g£¬ÕżČ·£»C”¢ČōŠæÖŹĮæ·ÖŹżĪŖ50%£¬ŌņŠæµÄÖŹĮæĪŖ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗÓ±±Ź”±ĻŅµÉśÉżŃ§ĪÄ»ÆæĪÖŹĮæ¼ģ²āĄķ×Ū£ØŅ»£©»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŹµŃéĢā
ĻĀĶ¼ŹĒŠ”Ć÷ÅäÖĘ100gÖŹĮæ·ÖŹżĪŖ10%µÄĒāŃõ»ÆÄĘČÜŅŗµÄŹµŃé²Ł×÷Ź¾ŅāĶ¼”£

(1)Öø³öĶ¼ÖŠµÄŅ»“¦Ć÷ĻŌ“ķĪó_________________________”£
(2)ÓĆÉĻŹöĶ¼Ź¾µÄŠņŗűķŹ¾ÅäÖĘČÜŅŗµÄ²Ł×÷Ė³Šņ£ŗ____________________________”£
(3)ÅäÖĘŗƵÄĒāŃõ»ÆÄĘČÜŅŗŅŖĆÜ·ā±£“ęµÄŌŅņŹĒ(ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾)£ŗ_______________”£
³ĘĮæŹ±ĒāŃõ»ÆÄĘĪ“·ÅŌŚ²£Į§Ę÷ĆóÖŠ(»ņĮæĖ®Ź±ŃöŹÓ¶ĮŹż) ¢Ü¢Ł¢Ū¢Ż¢Ś(»ņ¢Ū¢Ü¢Ł¢Ż¢Ś) 2NaOH+CO2=Na2CO3+H2O ”¾½āĪö”æ±¾Ģāæ¼²éĮĖŅ»¶ØČÜÖŹÖŹĮæ·ÖŹżµÄČÜŅŗµÄÅäÖĘ£¬Ć÷Č·ÅäÖĘŅ»¶ØČÜÖŹÖŹĮæ·ÖŹżµÄČÜŅŗŹµŃé²½Öč£Ø¼ĘĖć”¢³ĘĮ攢Čܽā”¢×°ĘæĢłĒ©£©”¢²Ł×÷×¢ŅāŹĀĻīµČŹĒÕżČ·½ā“š±¾ĢāµÄ¹Ų¼ü”£ £Ø1£©ĒāŃõ»ÆÄĘ¾ßÓŠøÆŹ“ŠŌ£¬³ĘĮæŹ±£¬ĒāŃõ»ÆÄĘŅŖ·ÅŌŚ²£Į§Ę÷ĆóÖŠ£¬Ķ¼ÖŠ·ÅŌŚÖ½ÉĻ£¬ĮæČ”ŅŗĢåŹ±£¬ŹÓĻßÓėŅŗĢåµÄ°¼ŅŗĆę×īµĶ“¦...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗÓ±±Ź”±ĻŅµÉśÉżŃ§ĪÄ»ÆæĪÖŹĮæ¼ģ²āĄķ×Ū£ØŅ»£©»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ×ö·ØÖŠ²»ÕżČ·µÄŹĒ
A. ÓĆ¼ÓµāŃĪ×÷µ÷Ī¶Ę· B. ÓĆ¼×Č©ČÜŅŗ±£ĻŹŗ£²śĘ·
C. ÓĆŠ”ĖÕ“ņ×÷·¢½Ķ·Ū D. »īŠŌĢæÓĆ×÷±łĻä³żĪ¶¼Į
B ”¾½āĪö”æA”¢¼ÓµāŃĪ¾ßÓŠĻĢĪ¶£¬¼ÓµāŃĪæÉÓĆ×÷µ÷Ī¶Ę·£¬ÕżČ·£»B”¢¼×Č©¶ŌČĖĢåÓŠŗ¦£¬Ź³ÓĆ¼×Č©ČÜŅŗ½žÅŻ¹żµÄŗ£²śĘ·£¬»įĪ£ŗ¦ČĖĢ彔浣¬“ķĪó£»C”¢Š”ĖÕ“ņŹÜČČ·Ö½āÉś³ÉĢ¼ĖįÄĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼£¬Ź¹øāµćŹčĖɶąæ×£¬±ŗÖĘøāµćŹ±¼ÓČėŠ”ĖÕ“ņÓĆ×÷·¢½Ķ·Ū£¬ÕżČ·£»D”¢»īŠŌĢæ¾ßÓŠĪüø½ŠŌ£¬æÉÓĆ×÷±łĻä³żĪ¶¼Į£¬ÕżČ·”£¹ŹŃ”B”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ¹óÖŻŹ”°²Ė³ŹŠ2018ÄźÖŠæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ¼ĘĖćĢā
ŌŚĻĀĆęĮ½×éĪļÖŹÖŠ£¬Ćæ×é¾łÓŠŅ»ÖÖÓėĘäĖūĪļÖŹĖłŹōĄą±š²»Ķ¬£¬ĒėŠ“³öÕāÖÖĪļÖŹµÄ»ÆѧŹ½²¢¼ĘĖćĘäĻą¶Ō·Ö×ÓÖŹĮ攣


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗɽ¶«Ź”ŗŹŌóŹŠ2018ÄźÖŠæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ¼ĘĖćĢā
ij»ÆѧŠĖȤŠ”×éĪŖĮĖ²ā¶Ø¼¦µ°æĒÖŠĢ¼ĖįøʵÄŗ¬Įæ,½ųŠŠĮĖČēĻĀŹµŃé:Č”25.0gĻ“¾»”¢·ŪĖéŗóµÄ¼¦µ°æĒѳʷ·ÅÓŚÉÕ±ÖŠ,ĻņÉÕ±ÖŠµĪ¼ÓĻ”ŃĪĖį(Õūøö¹ż³Ģ²»æ¼ĀĒŃĪĖįµÄ»Ó·¢ŗĶĘųĢåµÄČܽā),ŹµŃé²āµĆÉÕ±ÖŠŹ£ÓąĪļÖŹµÄÖŹĮæÓė¼ÓČėŃĪĖįµÄÖŹĮæÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾

Ēó:(1)²śÉśCO2µÄ×ÜÖŹĮæĪŖ____________g”£
(2)¼¦µ°æĒÖŠĢ¼ĖįøʵÄÖŹĮæ·ÖŹż________________”£
9.9 90%. ”¾½āĪö”放½āĪö”æ (1)øł¾ŻÖŹĮæŹŲŗć¶ØĀÉæÉÖŖ·“Ó¦Ē°ŗó¼õÉŁµÄÖŹĮæ¾ĶŹĒÉś³É¶žŃõ»ÆĢ¼µÄÖŹĮ棬²śÉśCO2µÄ×ÜÖŹĮæĪŖ25g+150g-165.1g=9.9g£»(2)Éč¼¦µ°æĒÖŠĢ¼ĖįøʵÄÖŹĮæŹĒx£¬Ōņ£ŗ CaCO3+2HClØTCaCl2+CO2”ü+H2O 100 44 x 9.9g x=22.5g£¬ ¼¦µ°æĒÖŠĢ¼ĖįøʵÄÖŹĮæ·ÖŹż=”Į100%=90%£¬ “š£ŗ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ŃĪ³ĒŹŠ2018ÄźÖŠæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗæĘѧĢ½¾æĢā
»ÆѧŌŚøÄÉĘČĖĄąÉś“ę»·¾³£¬ĢįøßÉś»īÖŹĮæ·½ĆęĘš×ÅÖŲŅŖ×÷ÓĆ”£
£ØøÄÉĘ»·¾³£©ĪĀŹŅŠ§Ó¦ŗĶĖįÓź»įĶžŠ²Éŗŗ÷½øÉś“ę”£ĪŅ¹śæŖÕ¹ĮĖÄĻŗ£Éŗŗ÷½øÉśĢ¬ŠŽø“¹¤×÷”£
(1)ĪŅĆĒ°ŃpH___(Ģī”°>”±”¢”°<”±»ņ”°=”±£©5.6µÄ½µÓź³ĘĪŖĖįÓź”£
(2)ĪŖøÄÉĘÉś“ę»·¾³£¬³«µ¼”°µĶĢ¼”±Éś»ī”£½ØŅéŹ¹ÓĆĒå½ąÄÜŌ“”£Š“³öŅ»ÖÖ³£¼ūµÄĒå½ąÄÜŌ“______”£
£ØĢ½²ā׏Ō“£©½üĘŚ£¬ĪŅ¹śĻņŌĀĒņ±³Ćę³É¹¦·¢ÉäŅ»æÅÖŠ¼ĢĶØŠÅĪĄŠĒ£¬ÖśĮ¦Ģ½²āŌĀĒņ׏Ō“”£
(1)ŌĀĒņÉĻÓŠ·įø»µÄŗĖÄÜŌĮĻHe-3”£HeµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ_____(Ģī×ÖĆæŠņŗÅ)”£
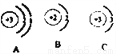
(2)ŌĀĒņĶĮČĄÖŠÓŠĢģČ»µÄĢś”¢ĀĮ”¢ŅųµČ½šŹōæÅĮ£”£øł¾ŻĢśŠāŹ“µÄĢõ¼ž·ÖĪö£¬ĢśŌŚŌĀĒņÉĻ²»Ņ׊āŹ“µÄŌŅņæÉÄÜŹĒ_____________”£
£ØŃŠ·¢²ÄĮĻ£©ÖŠ¹śŠ¾ÕĆĻŌÖŠ¹ś”°ÖĒ”±Ōģ”£Š¾Ę¬µÄ»ł²ÄÖ÷ŅŖŹĒøß“æ¹č”£
(1)¹čŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄŠÅĻ¢ČēĶ¼ĖłŹ¾£¬¾ŻĶ¼æɵƵ½µÄŠÅĻ¢ŹĒ______(Ģī×ÖÄøŠņŗÅ)”£

A.¹čŌŖĖŲŹĒ·Ē½šŹōŌŖĖŲ B.¹čŌŖĖŲµÄŌŖĖŲ·ūŗÅĪŖSi
C.¹čŌŖĖŲŌŚµŲæĒĄļµÄŗ¬ĮæÅŵŚ¶žĪ»
(2)ĻĀĶ¼ŹĒŅ»ÖÖÖʱøøß“æ¹čµÄ¹¤ŅÕĮ÷³ĢĶ¼£ŗ
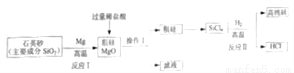
£Ø²éŌÄ׏ĮĻ£©³£ĪĀĻĀ£¬ĀČ»ÆĆ¾ČÜŅŗ³ŹÖŠŠŌ”£
¢Ł·“Ó¦IµÄ»Æѧ·½³ĢŹ½: 2Mg+SiO2 Si+2MgO£¬øĆ·“Ó¦ŹōÓŚ______ (Ģī»ł±¾·“Ó¦ĄąŠĶ)”£·“Ó¦IIŅŖŌŚĪŽŃõĘų»·¾³ÖŠ½ųŠŠ£¬ŌŅņŹĒ_______(“š³öŅ»ÖÖ¼“æÉ)”£
Si+2MgO£¬øĆ·“Ó¦ŹōÓŚ______ (Ģī»ł±¾·“Ó¦ĄąŠĶ)”£·“Ó¦IIŅŖŌŚĪŽŃõĘų»·¾³ÖŠ½ųŠŠ£¬ŌŅņŹĒ_______(“š³öŅ»ÖÖ¼“æÉ)”£
¢Ś²Ł×÷IµÄĆū³ĘŹĒ¹żĀĖ”£¹żĀĖŹ±ŅŗĆęÓ¦_____(Ģī”°øßÓŚ”±»ņ”°µĶÓŚ”±) ĀĖÖ½±ßŌµ”£ĖłµĆ“Ö¹čÓ¦³ä·ÖĻ“µÓ£¬ŅŌ³żČ„±ķĆęæÉÄÜŗ¬ÓŠµÄŃĪĖį”¢____ (Ģī»ÆѧŹ½)”£
¢Ū¼ņŅŖŠšŹö¼ģŃéŃĪĖįŅŃ¹żĮæµÄ·½·Ø_______”£
¢ÜÉĻŹöŅŃÖŖÉś²śĮ÷³ĢÖŠ£¬æÉŅŌŃ»·ĄūÓƵÄĪļÖŹŹĒ______(Ģī»ÆѧŹ½)”£
<£» Ģ«ŃōÄÜ B£» ŌĀĒņÉĻȱɣŃõĘųŗĶĖ® AB£» ÖĆ»»£¬ ·ĄÖ¹±¬Õأػņ·ĄÖ¹Éś³ÉµÄ¹č±»Ńõ»Æ£©£» µĶÓŚ£¬ MgCl2£» Č”ÉĻ²ćĒåŅŗ£¬¼ÓČėÉŁĮæNaHCO3ČÜŅŗ¹Ū²ģÄÜ·ń²śÉśĘųĢ壬Čō²śÉśĘųĢåŌņŃĪĖįŅŃ¹żĮæ HCl ”¾½āĪö”æ£Ø1£©pHŠ”ÓŚ5.6µÄÓźĖ®½ŠĖįÓź£» £Ø2£©Ģ«ŃōÄÜ”¢·ēÄÜ”¢Ė®ÄܵȏĒĒå½ąµÄÄÜŌ“£» ”¾Ģ½²ā׏Ō“”æ £Ø1£©ŗ¤ŹĒ2ŗÅŌŖĖŲ£¬¹ŹÖŹ×ÓŹżŹĒ2£¬¹ŹŌ×Ó½į¹¹Ź¾ŅāĶ¼ŹĒB£» £Ø2£©ŌĀĒņÉĻ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗÄŚĆɹŰüĶ·ŹŠ2018ÄźÖŠæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ¼ĘĖćĢā
ijŠĖȤŠ”½MĪŖ²ā¶ØŹÆ»ŅŹÆÖŠĢ¼ĖįøʵÄÖŹĮæ·ÖŹż£¬Č”12gŹÆ»ŅŹÆѳʷ¼ÓČėÉÕ±ÖŠ,½«120gĻ”ŃĪĖįĘ½¾ł·ÖĖÄ“Ī¼ÓČė£¬³ä·Ö·“Ó¦ŗó(ŌÓÖŹ²»ČÜÓŚĖ®Ņ²²»ÓėĻ”ŃĪĖį·“Ó¦)£¬²āµĆŹµŃ鏿¾ŻČēĻĀ£ŗ
ŹµŃé“ĪŹż | µŚŅ»“Ī | µŚ¶ž“Ī | µŚČż“Ī | µŚĖÄ“Ī |
¼ÓČėĻ”ŃĪĖįµÄÖŹĮæ/g | 30 | 30 | 30 | 30 |
Ź£Óą¹ĢĢåµÄÖŹĮæ/g | 9 | 6 | 3 | 2 |
·ÖĪöŹż¾Ż¼ĘĖć(½Y¹ū¾«Č·µ½0.1%)£ŗ
(1)øĆĻéĘ·ÖŠĢ¼ĖįøʵÄÖŹĮæ·ÖŹżĪŖ__________”£
(2)ĖłÓĆĻ”ŃĪĖįµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ__________”£
(3)12gѳʷ֊µÄĢ¼ĖįøĘĒ”ŗĆĶźČ«·“Ó¦Ź±ĖłµĆČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ__________”£
83.3% 7.3% 10.5% ”¾½āĪö”æ£Ø1£©ÓÉĶ¼æÉÖŖ£¬×īÖÕŹ£Óą¹ĢĢåµÄÖŹĮæĪŖ2g£¬¹Ź»ģŗĻĪļÖŠĢ¼ĖįøʵÄÖŹĮæĪŖ12g-2g=10g£¬¹ŹŃłĘ·ÖŠĢ¼ĖįøʵÄÖŹĮæ·ÖŹżĪŖ”Į100%=83.3% £» £Ø2£©ŅŌµŚŅ»“ĪµÄŹ¹ÓĆŹż¾ŻĪŖ×¼£¬Ćæ30gµÄĻ”ŃĪĖįæÉŅŌ·“Ó¦3gµÄĢ¼ĖįøĘ£¬Éč30gĻ”ŃĪĖįÖŠČÜÖŹµÄÖŹĮæĪŖx CaCO3+2HCl == CaCl2+H2O+CO2”ü 100 73 3 x ...²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com