
分析 根据方程式的反应物、产物、反应条件等进行分析相同点、不同点.
解答 解:(1)这三个方程式的共同点是:都有氧气产生;都是分解反应;反应物都含有氧元素等;
(2)不同之处有:①不需要加热,②③都需要加热;(或①反应物是液体,②③反应物是固体;或②的生成物有三种,①③生成物只有两种;或②不需要催化剂,①③需要催化剂;).
故答案为:(1)都有氧气生成;都是分解反应;
(2)①不需要加热,②③都需要加热;①反应物是液体,②③反应物是固体;或②的生成物有三种,①③生成物只有两种;或②不需要催化剂,①③需要催化剂.(答案合理即可)
点评 本题难度不大,能训练学生的发散思维能力,解题时从物质分类、反应物、生成物及反应类型的角度对比分析是解题的主要切入点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
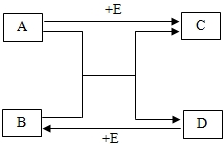 已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如图所示.如果A、B均为黑色固体,C是造成温室效应的主要气体,E是气态单质.则E的用途(请举一例)是供给呼吸,A与B反应的基本类型是置换反应.写出下列反应的化学方程式
已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如图所示.如果A、B均为黑色固体,C是造成温室效应的主要气体,E是气态单质.则E的用途(请举一例)是供给呼吸,A与B反应的基本类型是置换反应.写出下列反应的化学方程式查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子一定由原子构成 | B. | 原子中一定含有质子、中子和电子 | ||
| C. | 原子得到电子后会形成阴离子 | D. | 分子、原子、离子都可以构成物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com