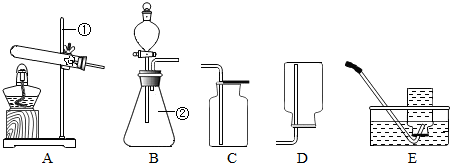
(2013?广陵区一模)SiO
2作为牙膏的高档摩擦剂具有洁齿能力强、理化性能好等特点,适于生产高档透明牙膏.如图是工业生产SiO
2的工艺流程图.请回答相关问题.
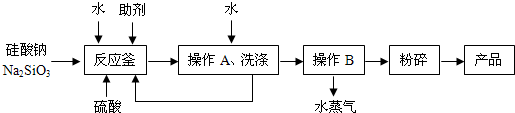
(1)反应过程中要不断搅拌且保持温度为80~95℃,目的是
使反应物充分接触并使反应充分进行并且反应进行快
使反应物充分接触并使反应充分进行并且反应进行快
;
(2)写出反应釜中发生反应的化学方程式
Na2SiO3+H2SO4═SiO2+Na2SO4+H2O
Na2SiO3+H2SO4═SiO2+Na2SO4+H2O
;
(3)上述反应生成物中,属于盐类物质的阴离子
SO42-
SO42-
(填离子符号);
(4)操作A的名称是
过滤
过滤
,若在实验室完成此实验,需要的玻璃仪器有烧杯、
漏斗
漏斗
和
玻璃棒
玻璃棒
;
(5)操作B的名称是
烘干或者干燥
烘干或者干燥
,为顺利完成此操作,通常将产品均匀铺开置于鼓风箱中,这样做的目的是
增加产品和空气的接触面积,以便产品快速干燥
增加产品和空气的接触面积,以便产品快速干燥
;
(6)检验产品已经洗涤干净的方法是
取最后一次洗涤液,蒸发,若无固体析出,则已经洗净;或取最后一次洗涤液,滴加硝酸钡(或氯化钡),若无沉淀生成,则已经洗净
取最后一次洗涤液,蒸发,若无固体析出,则已经洗净;或取最后一次洗涤液,滴加硝酸钡(或氯化钡),若无沉淀生成,则已经洗净
.