
分析 (1)根据金属活动性顺序,排在氢前面的金属能和酸反应,后面的金属不能和酸反应分析;
(2)根据排在前面的金属能把排在后面的金属从它的盐溶液中置换出来分析.
解答 解:(1)根据题意可知,R能与酸反应产生氢气,由金属R不可能是金属银;
(2)由于金属和酸反应产生的盐能与锌反应,可判断盐中金属活动性比锌弱,而金属镁的活动性比锌强,因此金属R应为铁,锌和硫酸亚铁反应生成硫酸锌和铁,化学方程式为:Zn+FeSO4=ZnSO4+Fe.
故答案为:(1)银;
(2)Zn+FeSO4=ZnSO4+Fe.
点评 本题属于金属活动性顺序的考查,依据金属活动性顺序中位于氢之前的金属能从酸中置换出氢,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来分析即可.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 固体硝酸铵溶于水,溶液的温度降低 | |
| B. | 镁条在空气中燃烧生成黑色固体 | |
| C. | 锌片加入稀硫酸中,产生大量的气泡 | |
| D. | 硫在氧气中燃烧发出蓝紫色火焰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
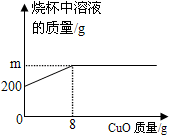 已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g.向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示.当恰好完全反应时,所得的溶液为不饱和溶液.
已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g.向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示.当恰好完全反应时,所得的溶液为不饱和溶液.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
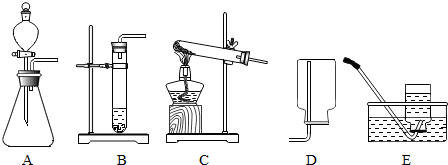
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
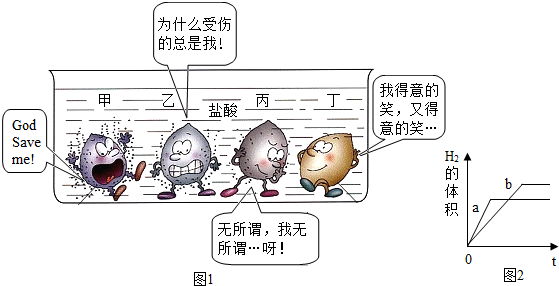
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 城市街道洒水降尘 | B. | 发展水力、风力发电 | ||
| C. | 露天焚烧秸秆、树叶 | D. | 乘坐公交车或地铁出行 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 每1个C原子和1个O2分子反应,生成2个CO2分子 | |
| B. | 32g S与32g O2完全反应,生成64g SO2 | |
| C. | 镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律 | |
| D. | 根据:蜡烛+氧气$\stackrel{点燃}{→}$二氧化碳+水,则蜡烛中一定含有C、H、O三种元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com