

| ʱ��/s | 0 | 5 | 10 | 15 |
| ����/g | 215.2 | 211.4 | 208.6 | 208.6 |
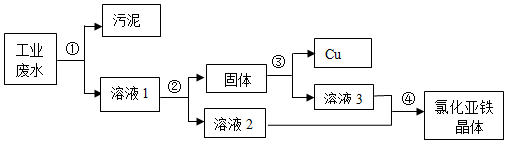
���� ��1�����ݴ�������ˮ��Һ�ʼ��Խ��н��
��2�������Ȼ��Ƶ��ܽ�����¶ȵ�Ӱ��仯������н��
��3�����ݰ�������ˮ�ʼ��Խ��н��
��4������̼�����Ƶ���;���н��
��5������̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼���н��
��6�������������ݿɼ������ɵĶ�����̼��������������ȫ��Ӧ�ų�������̼������������Ʒ��̼���Ƶ����������ɴ��жϸò�Ʒ��̼���Ƶ�����������
��� �⣺��1����������ˮ��Һ�ʼ��ԣ����Դ���ˮ��Һ�е�����ɫ��̪��Һ�Ժ�ɫ������죻
��2���Ȼ��Ƶ��ܽ�����¶ȵ�Ӱ��仯�������ԴӲ������ȡ���γ��������ᾧ��������������ᾧ��
��3����������ˮ�ʼ��ԣ������ڶ�����̼�����գ������������ˮ�ʼ��ԣ������ڶ�����̼�����գ�
��4��̼�����Ƶ���;�У�����θ����࣬�������ͷۣ��������θ����࣮
��5�������ȵ������£�̼�����Ʒֽ�������̼���ơ�ˮ�Ͷ�����̼��������Ӧ�Ļ�ѧԭ���ǣ�2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O���÷�Ӧ��һ�����ʷ�Ӧ���ɶ������ʣ����ڷֽⷴӦ�����2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O���ֽ⣻
��6���ٸ��ݱ������ݿɵã����ɶ�����̼������=215.2g-208.6g=6.6g�����6.6g��
�����Ʒ��̼���Ƶ�����Ϊx��
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 44
x 6.6g
$\frac{106}{x}$=$\frac{44}{6.6g}$
x=15.9g
�ò�Ʒ��̼���Ƶ���������=$\frac{15.9g}{16.5g}$��100%=96.4%
�𣺸ò�Ʒ��̼���Ƶ���������96.4%��
���� �������ʵ�飬��ѧ�ؽ���ʵ�顢����ʵ�飬�ǵó���ȷʵ����۵�ǰ�ᣬ���Ҫѧ�����ʵ�顢����ʵ�顢����ʵ�飬Ϊѧ�û�ѧ֪ʶ�춨������


 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д� ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C��CO2��CO | B�� | Fe2O3��Fe2��SO4��3��Fe��OH��3 | ||
| C�� | NaCl��NaNO3��NaOH | D�� | SO3��Na2SO4��BaSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼������Һ | B�� | �Ȼ�����Һ | C�� | ϡ���� | D�� | ������̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʯ | B�� | ʯ���� | C�� | ̼� | D�� | ��ľ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ÿ����������6��ԭ�ӹ��� | |
| B�� | ת�������Һͱ��ķ��Ӹ���֮��Ϊ1��1 | |
| C�� | ������Ԫ�ص���������С�ڶ� | |
| D�� | �ҡ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ʾ��һ�����ı����Ȼ�����Һ�м����Ȼ��ƹ��� | |
| B�� | 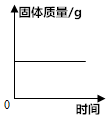 ��һ�����ĸ�����ع�����м��� | |
| C�� |  ��ʾ��ȫ��ͬ�����ݹ���������Һ���С����������·ֽ� | |
| D�� | 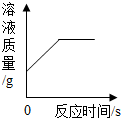 ��ʾ��һ��������ͭ��Һ�м���һ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
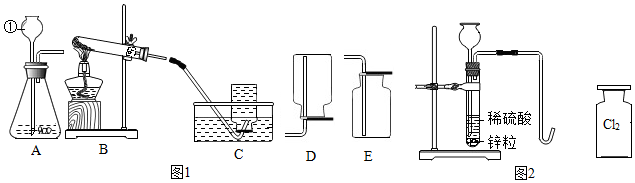
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʯī�����е����� | |
| B�� | ���÷���ˮ����Ӳˮ����ˮ | |
| C�� | ��������������ʢ�Ų�����Һ��������ͭ�� | |
| D�� | ��һ�������� CO2����ת��Ϊ CO |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com