
【题目】除去下列各物质中的少量杂质,所选用的试剂、方法都能达到目的的是( )
选项 | 物质 | 杂质(少量) | 操作方法 |
A |
|
| 将混合气体通过灼热的碳粉 |
B |
|
| 加入适量氢氧化钙溶液,过滤 |
C | 铁粉 |
| 加入适量的稀盐酸,过滤 |
D |
|
| 加入适量 |
A.AB.BC.CD.D
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图表示某些物质间转化关系(反应条件和部分产物已省略)。常温下A、C是由相同元素组成的无色液体,且A具有消毒杀菌作用;E是紫红色单质,D、I、J均为无色气体,其中I能使澄清的石灰水变浑浊;K为红棕色粉末。 请回答下列问题:

(1)反应①中B物质的作用是________;
(2)图中标出的反应①到⑦中是化合反应的是______________(填数字序号);
(3)写出D化学式的_______________________;
(4)反应②中的现象为______________;
(5)写出Ⅰ使澄清的石灰水变浑浊的化学方程式________________。
(6)写出反应③的方程式__________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝在工业和日常生活中应用广泛。请回答:
(1)铝元素的含量居地壳中所有元素的第______位。将铝块拉成细丝、压成薄片是利用铝的_______性。
(2)元素的化学性质与原子的最外层电子数有密切关系。下图为铝原子的结构示意图,铝原子在化学反应中容易_________(填“得到”或“失去”)电子,形成离子的符号为_____________。
![]()
(3)铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化,因此铝具有很好的抗腐蚀性能。写出铝与氧气反应的化学方程式:___________。
(4)冰晶石在工业制取金属铝的过程中起着重要的作用。硫酸铝和氟化钠(NaF)在共融条件下反应生成冰晶石(Na3AlF6),同时得到硫酸钠,写出此反应的化学方程式: _________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某氢氧化钠溶液与稀盐酸反应过程中的温度及pH变化:有关分析错误的是( )
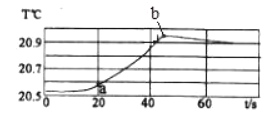
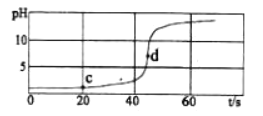
A.该实验是将氢氧化钠溶液滴入稀盐酸中
B.a点对应溶液的溶质为氯化钠和氯化氢
C.b点表示酸碱恰好完全中和
D.c点到d点的曲线变化证明该反应放热
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,操作的规范性在实验中尤为重要。下列图示的实验操作中,正确的是
A. 称量固体氢氧化钠B.
称量固体氢氧化钠B.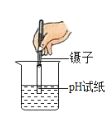 测溶液pH
测溶液pH
C.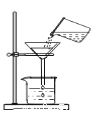 过滤D.
过滤D. 稀释浓硫酸
稀释浓硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题:
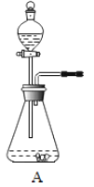
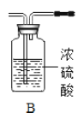



(1)若以石灰石和稀盐酸为原料,在实验室中制备并收集一瓶干燥纯净的二氧化碳气体。
①所选仪器的连接顺序为__________(从左至右填写仪器序号字母)。
②请写出装置A中所发生反应的化学方程式_________。
③性质决定用途,下列关于二氧化碳的用途主要利用其物理性质的是_______(填写序号A、B、C、D之一)。
A 二氧化碳可用于灭火
B 固体二氧化碳可用于人工降雨
C 二氧化碳可用作气体肥料
D 二氧化碳可用于生产碳酸氢钠
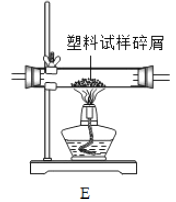
(2)第二组的同学以过氧化氢溶液为原料(![]() 为催化剂)制备氧气,并对某种塑料的组成元素进行分析探究(资料显示该塑料只含
为催化剂)制备氧气,并对某种塑料的组成元素进行分析探究(资料显示该塑料只含![]() 三种元素),所选仪器按“
三种元素),所选仪器按“![]() 碱石灰干燥管”的顺序连接,(
碱石灰干燥管”的顺序连接,(![]() 为浓硫酸洗气瓶),实验前检验装置气密性.使该塑料试样碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应),试回答下列问题:
为浓硫酸洗气瓶),实验前检验装置气密性.使该塑料试样碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应),试回答下列问题:
①仪器A中所发生反应的化学方程式为:____________。
②当仪器D中出现_________的现象时,则可证明塑料样品中含有碳元素。
③仪器E的玻璃管中放入的塑料试样碎屑质量为mg,塑料试样充分燃烧后,测得仪器![]() 质量增加ag,仪器
质量增加ag,仪器![]() 质量增加bg,仪器D质量增加cg,则mg该塑料试样中含氢元素的质量为________g,碳元素的质量为_______g(计算结果可为分数形式)。
质量增加bg,仪器D质量增加cg,则mg该塑料试样中含氢元素的质量为________g,碳元素的质量为_______g(计算结果可为分数形式)。
④若装置中没有连接仪器![]() ,这样测算出的该塑料试样中碳元素的质量与实际值比较将__________(填“偏小”“偏大”“基本一致”之一)。
,这样测算出的该塑料试样中碳元素的质量与实际值比较将__________(填“偏小”“偏大”“基本一致”之一)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)某燃料X在7.2g氧气中燃烧,得到9.2g混合气体(可能含有一氧化碳、二氧化碳、水蒸气)。化学兴趣小组的同学利用下图所示装置验证混合气体的成分。
资料:①浓硫酸具有吸水性。②浓氢氧化钠溶液能吸收二氧化碳。
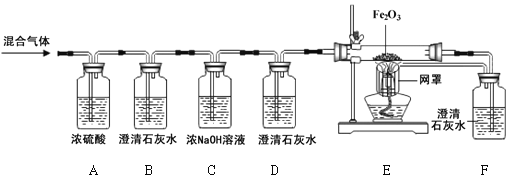
(1)通过混合气体后,A装置增重4.5g,说明混合气体中含有________________________。
(2)B装置中澄清石灰水变浑浊,发生反应的化学方程式为 。D装置的作用是 。
(3)当观察到 ,证明混合气体中有CO。
(4)实验结束后,同学们称量B、C装置共增重3.3g,根据以上数据可确定燃料X中所含元素及元素质量比为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸镁水合物是制备镁产品的中间体.
(制取MgCO33H2O)工业上从弱碱性卤水(主要成分为MgCl2)获取MgCO33H2O的方法如图1:
(1)沉淀过程的化学方程式为:MgCl2+CO2+2NaOH+2H2O═MgCO33H2O↓+2____.
(2)沉淀过程的pH随时间的变化如图2所示,沉淀过程的操作为___(填字母).
a 向卤水中滴加NaOH溶液,同时通入CO2
b 向NaOH溶液中滴加卤水,同时通入CO2
c 向卤水中通入CO2至饱和,然后滴加NaOH溶液,同时继续通入CO2
d 向NaOH溶液中通入CO2至饱和,然后滴加卤水,同时继续通入CO2

(3)沉淀过程的溶液中镁离子含量随时间的变化如图3所示,不同温度下所得到沉淀产物如下表所示.则沉淀过程选择的温度为____,理由是_______。
温度(℃) | 产物 |
46.95 | MgCO33H2O |
47.95 | MgCO33H2O |
48.95 | MgCO33H2O |
49.95 | Mg5(OH)2(CO3)44H2O |
(4)(测定MgCO33H2O的纯度)利用下图进行实验,以确定MgCO33H2O的纯度.
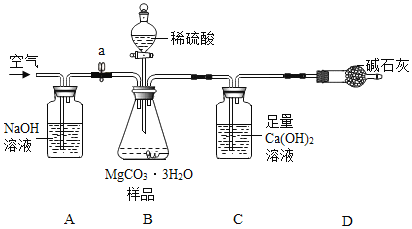
依据实验过程回答下列问题:
(5)实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有____。
(6)C中化学方程式为___;A中NaOH作用为___;D中碱石灰作用为____.
(7)下列各项措施中,不能提高测定准确度的是___(填标号).
a 在加入硫酸之前,应排净装置内的CO2气体 b 为了缩短实验时间,快速滴加硫酸
c 在A~B之间增添盛有浓硫酸的洗气装置 d 在C装置左侧导管末端增添多孔球泡
(8)实验中准确称取15.0g样品三份,进行三次测定,测得生成CaCO3沉淀的平均质量为10.0g.请计算样品中MgCO33H2O的纯度___(写出计算过程).
(9)小明认为应将澄清石灰水换成Ba(OH)2溶液,其理由除了Ba(OH)2溶解度大,浓度大,使CO2被吸收的更完全外,还有____.
(10)若获取MgCO33H2O的样品中含有少量Mg5(OH)2(CO3)44H2O,则产品中镁元素的质量分数__(填“偏大”“不变”或“偏小”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲乙丙丁四种物质的转化关系如图所示。下列说法正确的是

A.若丙为沉淀,则甲、乙中一定有一种物质是碱
B.若丙为气体,则甲、乙中一定有单质
C.若丁为水,则该反应一定是复分解反应
D.若甲、丁为单质,则该反应一定是置换反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com