
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:阅读理解
 (2012?泉州模拟)在初三化学实验复习课上,老师提供了三瓶无色溶液,其中一瓶是稀盐酸,另外两瓶没有贴标签,分别是碳酸钠溶液和氢氧化钠溶液.
(2012?泉州模拟)在初三化学实验复习课上,老师提供了三瓶无色溶液,其中一瓶是稀盐酸,另外两瓶没有贴标签,分别是碳酸钠溶液和氢氧化钠溶液.| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ.取少量B烧杯中的回收液于试管中,滴入饱和氢氧化钙溶液. | 产生白色沉淀 | B烧杯中的回收液中含有 碳酸钠 碳酸钠 |
| Ⅱ.①另取少量B烧杯中的回收液于试管中,滴入足量的 CaCl2 CaCl2 溶液.②过滤,往滤液中滴加 酚酞试液 酚酞试液 |
①产生白色沉淀. ② 酚酞变红色(或无变化) 酚酞变红色(或无变化) |
B烧杯中的回收液中 有氢氧化钠(或没有氢氧化钠) 有氢氧化钠(或没有氢氧化钠) |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
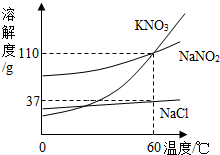 (2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.
(2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 项目 | 亚硝酸钠 | 氯化钠 |
| 化学式 | NaNO2 | NaCl |
| 色、态 | 白色固体 | 白色固体 |
| 水溶性 | 易溶 | 易溶 |
| 熔点 | 271℃ | 801℃ |
| 热稳定性 | 320℃发生分解,放出有臭味气体 | 1423℃熔化 |
| 水溶液的酸碱性 | 呈碱性 | 呈中性 |
| 跟稀盐酸作用 | 放出红棕色气体 | 无反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解的质量/g | 3.6 | 10.9 | 2.15 | 0.96 |
| 实验步骤和现象 | 实验结论 | 涉及到的化学方程式 |
| ① 取一支试管加入少量待测液,再滴加适量的稀盐酸,无明显现象 取一支试管加入少量待测液,再滴加适量的稀盐酸,无明显现象 |
该溶液不是碳酸钠溶液 该溶液不是碳酸钠溶液 |
NaOH+HCl═NaCl+H2O NaOH+HCl═NaCl+H2O |
| ② 另取一支试管加入少量待测液,再滴加几滴无色酚酞溶液,溶液变为红色 另取一支试管加入少量待测液,再滴加几滴无色酚酞溶液,溶液变为红色 |
该溶液为氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
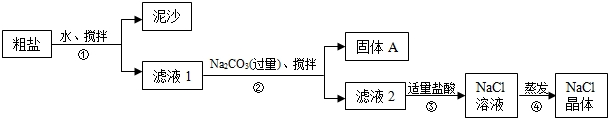
| 猜想 | 验证方法 | 实验现象 | 结论 |
| 猜想1: 固体A中含CaCO3 |
取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口. | 有气泡产生,石灰水变浑浊 有气泡产生,石灰水变浑浊 |
猜想1成立 |
| 猜想2: 固体A中含BaCO3 |
取少量固体A于试管中,先滴入 加入过量的稀盐酸 加入过量的稀盐酸 ,再滴入Na2SO4 Na2SO4 溶液. |
有气泡放出,无白色沉淀 | 第二种猜想不成立 第二种猜想不成立 |
| 猜想3: 最后制得的NaCl晶体中还含有Na2SO4 |
取少量NaCl晶体于试管中,加适量蒸馏水溶解,再 加酸化的BaCl2或Ba(NO3)2溶液 加酸化的BaCl2或Ba(NO3)2溶液 . |
有白色沉淀生成 有白色沉淀生成 |
猜想3成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com