
用右图的装置来测定空气中氧气的体积 分数。
分数。

(1)盛放在燃烧匙内的物质可用_____________。
(2)实验中观察到的现象是_____________,同时水进入广口瓶,水的体积约占广口瓶容积的_____________。
(3)如果实验步骤是:①先用夹子夹紧橡皮管;②点燃燃烧匙内的固体物质;③将燃烧匙插入广口瓶,并塞紧橡皮塞;④燃烧完毕后,打开橡皮管上的夹子,结果发现测定的氧气体积分数低于21%。问:这可能是由哪几 种原因引起的?
种原因引起的?
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:初中化学 来源: 题型:阅读理解
下表是某城市某日空气质量报告:
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | S02 | Ⅱ | 良 |
某研究性学习小组对表中首要污染物S0:导致酸雨的成因进行探究。
(提示:S02:是一种无色、有刺激性气味的有毒气体,易溶于水,具有与C0:相似的化学性质)
【探究实验】实验一:用下图所示装置进行实验。
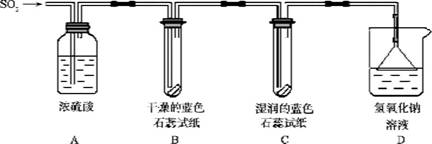
(1)A装置的作用是__________ S02气体。
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试
纸变红色,说明S02与水反应生成一种 _________________。
(3)D装置的作用是__________,发生反应的化学方程式是 ______________。
实验二:往盛有水的烧杯中通人S02气体,测所得溶液的pH ______ 7(填“>”“=”
或“<”),然后每隔l小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空
气中的氧气氧化最终生成H2S04。
【查阅资料】S02形成酸雨的另一途径:S02与空气中的02在飘尘的作用下反应生成S03
(飘尘的质量和性质在反应前后不发生变化),S03溶于降水生成H2S04。在此过程中飘尘作______________ 。
【探究结论】S02与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,因此酸雨对大理石的作用可以通
过大理石碎片放在醋中来模拟。当把2.0 g大理石碎片放在醋中一整夜后,取出固体干燥
称重,其质量可能是(醋酸钙易溶于水) __________。
A.小于2.0 g B.正好2.0 g C.大于2.0 g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,其实验的目的是
_____________
【知识联想】S02具有与C0:相似的化学性质,根据右图给出
的S02及其化合物问的相互转化关系回答:X的化学式是_____,写出X与Na2S03反应的化学方程________________________________,反应类型是_________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com