
【题目】微粒结构示意图是初中化学常见的示意图。现有下列微粒结构示意图,根据题意回答问题:

(1)写出沼气主要成分的化学式_____________。
(2)写出人体中含量最多金属元素的离子符号____________。
(3)写出雪碧、可乐等饮料中含有的一种酸的化学式____________。
(4)写出一种可用于中和胃酸过多的碱的化学式____________。
(5)写出六大营养素中最简单营养素的化学式____________。
科目:初中化学 来源: 题型:
【题目】第32届夏季奥运会将在日本东京举行,其奖牌制作的原料来自于电子垃圾中提炼出来的金属。从废线路板中提炼贵重金属和制备硫酸铜晶体的一种工艺流程如下:
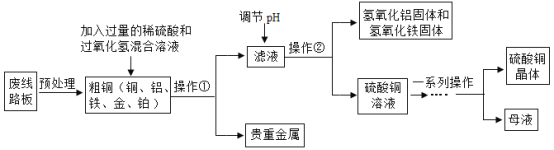
已知:在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
(1)操作②的名称是________;
(2)提炼出的贵重金属可制作奖牌,其成分是______________;
(3)“调节pH”时加碱液会使溶液的pH________(填“增大”或“减小”),其主要目的是除去滤液中Al3+和______(填金属离子符号);
(4)写出粗铜中的铜与稀硫酸和过氧化氢的混合溶液发生反应的化学方程式:__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019 年诺贝尔化学奖颁给了约翰·古迪纳夫、斯坦利·威廷汉和吉野彰三位科学家,以表彰他们在锂离子电池领域的卓越贡献。下图是锂元素在周期表中的部分信息及原子结构示意图。下列说法正确的是
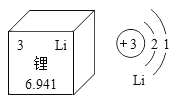
A.锂原子的核电荷数为 1
B.锂原子在化学反应中容易失去一个电子
C.锂元素的相对原子质量为 6.941 g
D.氯化锂的化学式为LiCl2
查看答案和解析>>
科目:初中化学 来源: 题型:
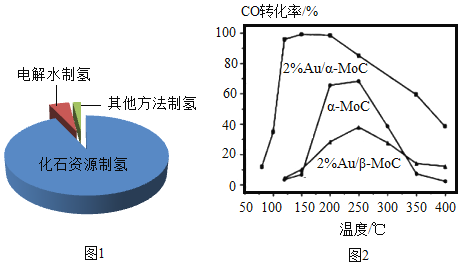
【题目】阅读下面科普短文。氢能是公认的高热值清洁能源。目前,氢气的来源如图1所示。化石资源制氢最为成熟。水煤气变换反应: ,是化石资源制氢过称中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
,是化石资源制氢过称中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我囯“人造太阳”大科学装置“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题。
(1)目前氢气的主要来源是_____。
(2)图2中,催化剂为2%Au/a-MoC时,CO转化率和温度的关系是_______。
(3)根据下表信息可知氘、氚都属于氢元素,理由是________。
原子种类 | 质子数 | 中子数 | 核外电子数 |
氘 | 1 | 1 | 1 |
氚 | 1 | 2 | 1 |
(4)下列说法正确的是___(填序号)。
A a-MoC可使CO转化率接近100%
B 水电解制氢的不足是造价高昂
C 利用太阳能制氢是未来发展方向
D “东方超环”利用核聚变提供能量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸钙为白色固体,易溶于水,可作食品防霉剂,国家标准规定了其用于制作面食、糕点时每千克面粉中的最大使用量。小组同学实验探究其性质和防霉的效果。
I.探究丙酸钙的性质
(进行实验)用下图裝置(夹持仪器已略去)完成实验,记录如下:
序号 | ① | ② |
装置 |
|
|
现象 | 试管内壁有水雾 | 注入酸后,有气泡产生,石灰水变浑浊 |
(解释与结论)
(1)②中现象说明有CO2产生。CO2与石灰水反应的化学方程式为________。
(2)查阅资料得知丙酸钙与盐酸反应无气体生成。由实验②可得出的结论是_______。
Ⅱ.探究丙酸钙防霉的效果
(进行实验)分别按下列①~⑧的配方蒸制8个馒头,冷却后置于密封袋中,记录如下:
组别 | 第1组 | 第2组 | |||||||
序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
配方 | 面粉/ g | 50 | 50 | 50 | 50 | 50 | 50 | 50 | 50 |
酵母/ g | 0.75 | 0.75 | 0.75 | 0.75 | 0.75 | 0.75 | 0.75 | 0.75 | |
蔗糖/ g | 0 | 0 | 0 | 0 | 5 | 5 | x | 5 | |
丙酸钙/g | 0 | 0.06 | 0.10 | 0.15 | 0 | 0.06 | 0.10 | 0.15 | |
开始发霉时间 | 第3天 | 第4天 | 第5天 | 第6天 | 第3天 | 第4天 | 第5天 | 第6天 | |
(解释与结论)
(3)设计第1组实验的目的是____。
(4)第2组,⑦中x为_______。
(5)对比第1组、第2组实验可得到的结论是______。
(反思与评价)
(6)某同学认为“制作面食、糕点时,丙酸钙用量越大越好”你是否同意此观点,并说明理由:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~F为初中化学常见的物质,它们之间有如图所示的转化关系,“→”表示物质间存在着相应的转化关系,“一”表示物质间能发生反应(部分反应物、生成物和反应条件未标出)。这些物质中只有A、B由两种元素组成,在空气中E的表面生成一层致密的氧化膜,因此E具有很好的抗腐蚀性能,F为紫红色固体。请分析后回答:

(1)E在空气中生成的氧化膜的化学式为___________。
(2)D→F的基本反应类型为________反应。
(3)写出A与B反应的化学方程式___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com