某种无色液体A和某种黑色粉末B混合后加热,生成无色液体C和无色气体D;另取一种黑色固体E,点燃后放入D中,发出白光,放出大量的热,只生成无色的气体F,某绿色粉末G加热分解也能生成F
(1)请分别写出A、C、D、F的名称:
A 、C 、D 、F ;
(2)黑色物质B在反应中起 作用,写出该反应的文字表达式 ;
(3)写出E和D反应生成F的文字表达式 ;该气体通入滴有紫色石蕊试液的蒸馏水中,会使紫色石蕊试液变 ,文字表达式 ;
(4)出土的古铜器表面常常有G,写出G的名称 .
【答案】
分析:根据黑色固体E,点燃后放入D中,发出白光,放出大量的热,说明D是氧气,则无色液体A是双氧水,B是二氧化锰,据此分析解答即可;
解答:解:根据黑色固体E,点燃后放入D中,发出白光,放出大量的热,说明D是氧气,则无色液体A是双氧水,B是二氧化锰,二氧化锰是该反应的催化剂,由于该反应的产物是水和氧气,所以C是水,根据E在氧气中燃烧的现象可知E是碳,F是二氧化碳,由某绿色粉末G加热分解也能生成F,所以G是碱式碳酸铜;
(1)由分析知A是双氧水,C是水,D是氧气,F是二氧化碳;
(2)二氧化锰在双氧水分解的反应中所起的作用是催化作用,该反应的表达式是双氧水
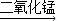
水+氧气;
(3)碳在氧气中燃烧会生成二氧化碳,其反应表达式为碳+氧气

二氧化碳;二氧化碳能与水反应生成碳酸,碳酸能使紫色的石蕊试液变红,二氧化碳与水的反应表达式为:水+二氧化碳→碳酸;
(4)有分析以及古铜器表面常常有G,所以可确定G是碱式碳酸铜;
故答案为:(1)双氧水;水;氧气;二氧化碳;
(2)催化;双氧水
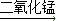
水+氧气;
(3)碳+氧气

二氧化碳;红色;水+二氧化碳→碳酸;
(4)碱式碳酸铜;
点评:推断习题要善于根据习题中的信息来寻找突破口,抓住解决问题的关键,比如本题中的颜色和状态可很快猜测是硫的燃烧和过氧化氢分解制氧气.

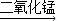 水+氧气;
水+氧气; 二氧化碳;二氧化碳能与水反应生成碳酸,碳酸能使紫色的石蕊试液变红,二氧化碳与水的反应表达式为:水+二氧化碳→碳酸;
二氧化碳;二氧化碳能与水反应生成碳酸,碳酸能使紫色的石蕊试液变红,二氧化碳与水的反应表达式为:水+二氧化碳→碳酸;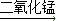 水+氧气;
水+氧气; 二氧化碳;红色;水+二氧化碳→碳酸;
二氧化碳;红色;水+二氧化碳→碳酸;
