
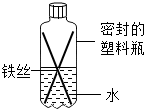
 如图为某化学兴趣小组设计的观察铁制品锈蚀的实验装置,请你分析,以下相关叙述中正确的是( )
如图为某化学兴趣小组设计的观察铁制品锈蚀的实验装置,请你分析,以下相关叙述中正确的是( )| A. | 此实验设计必须在玻璃仪器中进行 | |
| B. | 一段时间后,塑料瓶会变瘪,说明铁生锈与空气无关 | |
| C. | 一段时间后,铁丝会由下到上出现锈蚀现象 | |
| D. | 一段时间后,水面处铁丝锈蚀严重,而水上、水下部分生锈没有水面处严重 |
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:初中化学 来源: 题型:解答题
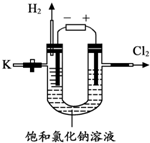 某学习小组对课本中“氯化钠能用于制烧碱”的内容产生兴趣,查阅资料得知:
某学习小组对课本中“氯化钠能用于制烧碱”的内容产生兴趣,查阅资料得知:
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CH4•H2O晶体中水是溶剂 | B. | CH4•H2O的组成元素有三种 | ||
| C. | 可燃冰是一种纯净物 | D. | 可燃冰燃烧说明水具有可燃性 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 为了保持身材只吃蔬菜,不吃肉类食物 | |
| B. | 食品添加剂可以使用,但必须按规定限量使用 | |
| C. | 要妥善保存食物,霉变食物中大多含有霉菌毒素,绝对不能食用 | |
| D. | 香烟的烟雾中含有多种有害物质,青少年应远离烟草 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间min | 0 | 2 | 4 | 6 | 8 | 10 |
| 质量/g | 0 | 0.7 | 1.1 | 1.5 | 1.7 | 1.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 验证 | 对比实验 | |
| 实验(示例) | 实验(仿照示例填写) | |
| 假设1 | 加热烧杯,烧杯不可燃 | (1)点燃蜡烛,蜡烛可燃 |
| 假设2 | 常温放置蜡烛,蜡烛不燃烧 | 加热蜡烛,蜡烛燃烧 |
| 假设3 | 点燃蜡烛,蜡烛在空气中持续燃烧 | 将燃着的蜡烛罩上一个烧杯,蜡烛熄灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
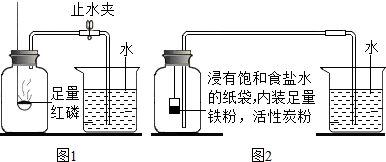
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 ,该原子在化学反应易失去(填“得到”或“失去”)电子,说明元素的化学性质与原子的最外层电子数关系密切.
,该原子在化学反应易失去(填“得到”或“失去”)电子,说明元素的化学性质与原子的最外层电子数关系密切.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com